
| n |
| V |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、上述过程的氧化剂为H2O2 | ||
B、若上述过程中产生的氧气为1mol,则消耗的H2CrO4为
| ||
| C、上述过程中Cr(OH)3是反应物 | ||
| D、上述过程的氧化产物为H2CrO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A的平衡浓度一定比原来平衡时大 |
| B、B的平衡浓度一定比原来平衡时小 |
| C、C的百分含量可能比原来平衡时大 |
| D、A的转化率一定比原来平衡时大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
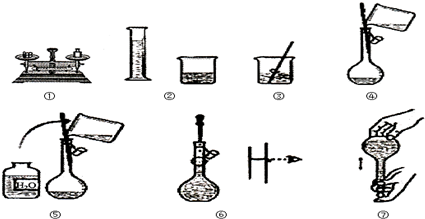
| A、②④ | B、①③⑤⑦ |
| C、①④⑥⑧ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖可用于补钙药物的合成 |
| B、二氧化硫可广泛用于食品的漂白 |
| C、聚乙烯塑料制品可用于食品的包装 |
| D、次氯酸钠溶液可用于环境的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 铜及其化合物在生活、生产中有广泛应用.请回答下列问题:
铜及其化合物在生活、生产中有广泛应用.请回答下列问题:
| ||
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、120 mL |
| B、60 mL |
| C、40 mL |
| D、30 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com