
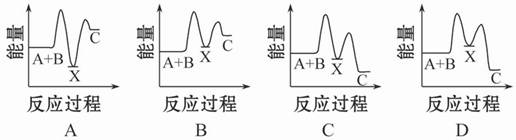
反应A+B→C(ΔH<0)分两步进行:①A+B→X(ΔH>0),
②X→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
科目:高中化学 来源: 题型:
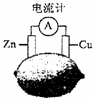
将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转.下列针对该装置的说法正确的是( )
|
| A. | 将电能转换为化学能 | B. | 电子由铜片流出 |
|
| C. | 锌片是负极 | D. | 铜片逐渐被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,当单独改变可逆反应N2+3H2 2NH3(正反应为放热反应)的下列条件后,有关的叙述中错误的是( )
2NH3(正反应为放热反应)的下列条件后,有关的叙述中错误的是( )
A.加入催化剂,v(正)、v(逆)都发生变化,且变化的倍数相等
B.增大压强,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.降低温度,v(正)、v(逆)都减小,且v(逆)减小的倍数大于v(正)减小的倍数
D.加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
查看答案和解析>>
科目:高中化学 来源: 题型:
如图a、b、c、d均为石墨电极,通电进行电解(电解液足量)下列说法正确的是
A. 向乙中加入适量盐酸,溶液组成可以恢复
B. 电解时向乙滴入酚酞溶液,c电极附近变红
C. 当b极有64gCu析出时,c电极产生2g气体
D.甲中a极上的电极反应为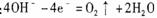
查看答案和解析>>
科目:高中化学 来源: 题型:
以化学反应原理为依据,以实验室研究为基础,可以实现许多化工生产。
I分解水制取氢气的工业制法之一是“硫-碘循环法”,主要涉及下列反应:

分析上述反应,下列判断正确的是____。
循环过程中产生1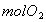 的同时产生
的同时产生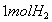
反应①中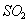 还原性比
还原性比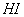 强
强
循环过程中需补充
反应③易在常温下进行
在一定温度下,向2L密闭容器中加入 ,发生反应②.物质的量随时间的变
,发生反应②.物质的量随时间的变 化如图所示。
化如图所示。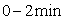 内的平均反应速率
内的平均反应速率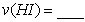
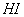 的转化率=_______
的转化率=_______
恒温恒容条件下,硫发生转化的反应过程和能量关系如图所示。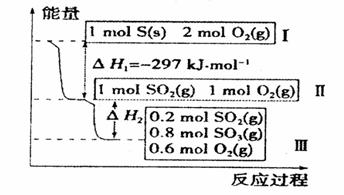 请回答下列问题:
请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式_______;
②恒温恒容时,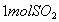 和
和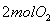 充分反应,放出热量的数值比
充分反应,放出热量的数值比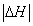 _____(填“大”、“小”或“相等”)
_____(填“大”、“小”或“相等”)
II.氮化硅(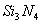 )是一种新型陶瓷材料,工业上有石英与焦炭在高温的氮气流中,通过以下反应制得:
)是一种新型陶瓷材料,工业上有石英与焦炭在高温的氮气流中,通过以下反应制得:

该反应平衡常数的表达式为K=_______.升高温度,其平衡常数
_________(填“增大”、“减少”或“不变”)。
(2)该化学反应速率与反应时间的关系如图所示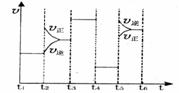
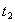 时引
时引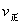 起突变的原因是_____,
起突变的原因是_____,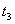 引起变化的因素是_____,
引起变化的因素是_____,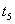 时引
时引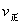 小变化、
小变化、 大变化的原因是_________.
大变化的原因是_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容条件下化学反应:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
ΔH=-Q kJ·mol-1在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是( )
A.在上述条件下反应生成1 mol SO3固体放热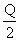 kJ
kJ
B.2Q3<2Q2=Q1<Q
C.Q1=2Q2=2Q3=Q
D.2Q2=2Q3<Q1<Q
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不正确的是
A.H、D、T互为同位素
B.NaHCO3、HCOONa均含有离子键和共价键
C.常温常压下,22.4 L CCl4含有NA个CCl4分子
D.常温下,23 g NO2含有NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度和pH。则电解过程中转移的电子的物质的量为
( )
A.0.1 mol B.0.2 mol C.0.3 mol D.0.4 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com