

| Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
| ��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
���� ���̿���ϡ���������MnCO3��FeCO3��Cu2��OH��2CO3�����ᷴӦ��SiO2�������ᷴӦ�����˵õ�����1ΪSiO2����Һ1�к�������þ����������������ͭ��ʣ���ϡ���ᣬ����Һ�м�����ʯ�ң�������ҺpH=4�����ö������������������½���Һ��Fe2+����ΪFe3+����PH=4ʱ�����õ�Fe3+ת��ΪFe��OH��3���������˳�ȥ����Һ2�м���MnS������Һ��Cu2+����ΪCuS�������˳�ȥ����Һ3��ΪMnCl2��ϵ��ת���õ�MnO2��
��1��MnCO3��FeCO3��Cu2��OH��2CO3�����ܽ���ϡ�������ɿ�����ˮ���Σ���SiO2������ˮ�Ҳ����ܽ���ϡ���̼���������ᷴӦ���������̡�������̼��ˮ������̼����������ˮ���ݴ�д���˷�Ӧ�����ӷ���ʽ��
��2���μ��Լ�1��Ŀ����Ϊ�˽���Һ��Fe2+����ΪFe3+��ͬʱ���Dz������µ����ʣ���ѡ��MnO2�������������£�MnO2����ԭΪMn2+������Һ��Fe2+����ΪFe3+����ϵ����غ㡢����غ㼰ԭ���غ�д��������Ӧ�����ӷ���ʽ��Fe3+��ȫ����ʱ��pHΪ3.7����Cu2+��ʼ����ʱ��pHΪ4.7���ݴ˷���������ҺpH�ķ�Χ��
��3��MnS������ͭ��Ӧת�������ܵ�CuS��ͬʱ�õ�����þ���˷�Ӧ��ƽ�ⳣ��K=$\frac{c��C{u}^{2+}��}{c��M{n}^{2+}��}$��
��4���������֪����������������Ӧ��������ʧȥ���ӷ���������Ӧ����MnO2���������ܽ�ʱ�������Ȼ�þ�ڵ��ʱ�����������ӷŵ�����������
��� �⣺���̿������������MnCO3��FeCO3��Cu2��OH��2CO3�����ᷴӦ��SiO2���������ᷴӦ�����˵õ�����1ΪSiO2����Һ1�к�������þ����������������ͭ��ʣ���ϡ���ᣬ����Һ�м�����ʯ�ң�������ҺpH=4�����ö������������������½���Һ��Fe2+����ΪFe3+����PH=4ʱ�����õ�Fe3+ת��ΪFe��OH��3���������˳�ȥ����Һ2�м���MnS������Һ��Cu2+����ΪCuS�������˳�ȥ����Һ3��ΪMnCl2��ϵ��ת���õ�MnO2��
��1����SiO2������ˮ�Ҳ����ܽ���ϡ���ᣬ�����̿���ϡ�����ܽ����������ΪSIO2��̼���������ᷴӦ���������̡�������̼��ˮ��������Ӧ�����ӷ���ʽΪ��MnCO3+2H+=Mn2++CO2��+H2O��
�ʴ�Ϊ���������裻MnCO3+2HCl=MnCl2+CO2��+H2O��
��2����ϲ������µ����ʣ�Ӱ���Ʒ�Ĵ��ȣ�ͬʱ���ܽ���Һ��Fe2+����ΪFe3+����ѡ��MnO2�������������·�����Ӧ�����ӷ���ʽΪ�����Fe3+��Cu2+�����������������pH��֪��������Һ3.7��pH��4.7������ʹFe3+��ȫ��������Cu2+��������
�ʴ�Ϊ��C��MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��3.7��pH��4.7��
��3��MnS������ͭ��Ӧת�������ܵ�CuS��ͬʱ�õ�����þ����Ӧ���ӷ���ʽΪ��MnS+Cu2+=Mn2++CuS���˷�Ӧ��ƽ�ⳣ��K=$\frac{c��C{u}^{2+}��}{c��M{n}^{2+}��}$=$\frac{{K}_{sp}��CuS��}{{K}_{sp}��MnS��}$=$\frac{1.95��1{0}^{-13}}{1.3��1{0}^{-36}}$=1.5��1023��
�ʴ�Ϊ��MnS+Cu2+=Mn2++CuS��1.5��1023��
��4���ö��Ե缫��������̺�����ػ����Һ�ķ���������ȡ������أ����ʱ��������ӦʽΪMn2+-2e-+2H2O=4H++MnO2����ҵ���������ܽ�̼���̣������������ܽ⣬��ԭ���������ӷŵ������ж�������������SO42-���ᣬ
�ʴ�Ϊ��Mn2+-2e-+2H2O=4H++MnO2�������ӷŵ������ж�������������SO42-���ᣮ
���� ���⿼����������ᴿ�������Ʊ�ʵ�飬Ϊ��Ƶ���㣬����ʵ�������еķ�Ӧ�����������ᴿ�����ԭ��Ϊ��� �Ĺؼ����ۺ��Խ�ǿ�����ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ����ç�����������3������̼ԭ�ӣ�
����ç�����������3������̼ԭ�ӣ�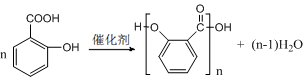 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ӻ�ˮ�и���þԪ����NaOH������ | |
| B�� | ��ˮ�����ķ�����Ҫ���������ӽ������͵��������� | |
| C�� | �Ӻ�ˮ����ȡ�嵥�ʵĹ���������������ԭ�� | |
| D�� | �������ճɻң���ˮ���ݣ��Ҵ���ȡ������ȡ�ⵥ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
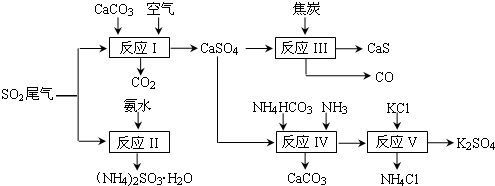
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2=CH2+HCl$\stackrel{����}{��}$CH3CH2Cl �Ӿ۷�Ӧ | |
| B�� | CH3COOH+CH3CH2OH?CH3COOCH2CH3+H2O ������Ӧ | |
| C�� |  �ӳɷ�Ӧ �ӳɷ�Ӧ | |
| D�� |  ȡ����Ӧ ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ��ƺͽ��ʯ | B�� | ��������Ͷ������� | ||
| C�� | ���ɱ� | D�� | �����Ͷ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C�������� | B�� | Al2O3����ԭ�� | ||
| C�� | N2������ԭ��Ӧ | D�� | AlN��������Ӧ�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�������ȷ�Ӧ | |
| B�� | �����ǽ���ѧ��ת��Ϊ���ܵ�һ��װ�� | |
| C�� | ��ѧ��Ӧ�������ı仯������Ϊ��������ʽ | |
| D�� | ˮ�������ǽ���ѧ��ת��Ϊ���ܵĹ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com