
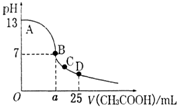
 室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )| A. | 全部正确 | B. | ①② | C. | ①③ | D. | ②④ |
分析 ①根据溶液中的电荷守恒判断;
②a=12.5时,氢氧化钠和醋酸溶液按照物质的量之比1:1反应生成的CH3COONa为强碱弱酸盐,溶液显碱性,pH>7;
③C点时,醋酸过量,溶液的组成为醋酸和醋酸钠的混合物,溶液显酸性,泽尔c(H+)>c(OH-),结合电荷守恒判断;
④在D点时,反应后溶质为等浓度的醋酸和醋酸钠,溶液呈酸性,则醋酸的电离程度等于醋酸根离子的水解程度,则c(CH3COO-)>(CH3COOH).
解答 解:①在A、B间任一点的溶液中都满足电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故①正确;
②a=12.5时,醋酸和氢氧化钠的物质的量之比为1:1,反应后溶液的组成为醋酸钠,CH3COONa为强碱弱酸盐,溶液显碱性,溶液的pH>7,应该介于AB之间,故②错误;
③C点时,醋酸过量,溶液的组成为醋酸和醋酸钠的混合物,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可得:c(CH3COO-)>c(Na+),溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故③正确;
④在D点时,反应后溶质为等浓度的醋酸和醋酸钠,由于醋酸的电离程度等于醋酸根离子的水解程度,则c(CH3COO-)>(CH3COOH),故④错误;
故选D.
点评 本题考查了酸碱混合的定性判断、离子浓度大小比较,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用方法.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol CH3+(碳正离子)中含有质子数为8NA | |
| B. | 6.4gCu与足量的硫反应,转移电子数为0.2 NA | |
| C. | 标准状况下,将分子总数为NA的NH3和HCl的充分混合后,所得混合气体体积越为22.4L | |
| D. | 7.8g Na2O2中含有的离子总数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和O2 | B. | Ca(OH)2和CO2 | C. | NaOH和HCl | D. | Na2CO3和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 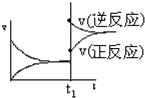 | C. | 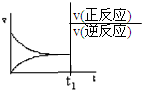 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0.70 | |
| T2 | 0.25 |
| A. | 上述信息可推知:T1<T2 | |
| B. | T1℃时,该反应的平衡常数K=$\frac{9}{16}$ | |
| C. | T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小 | |
| D. | T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com