
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. ![]() 的溶液中:Na+、K+、SiO32—、SO32-
的溶液中:Na+、K+、SiO32—、SO32-
B. pH=1的溶液中:K+、Al3+、SO42-、F—
C. 与镁反应生成氢气的溶液中:Na+、Ba2+、NO3-、Cl-
D. 0.1mol/L的NaHCO3溶液中:NH4+、Mg2+、Br-、AlO2-
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】一个体重50kg的健康人体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。请回答下列问题:
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____________。
A .Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中__________是氧化剂,说明维生素C具有 性。
(3)在人体中进行Fe2+![]() Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
(4)市场上出售的某种麦片中含有微量的颗粒细小的还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为___________________________,离子方程式为_________________________。
(5)己知下列反应:
①H2O2+2Fe3+=2Fe2++O2↑+2H+②2Fe2++H2O2+2H+=2Fe3++2H2O
反应①中生成1 molO2转移电子的物质的量为__________,反应①、②的总反应方程式为______________________,
在该反应中Fe3+的作用为________________。
(6)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中, HNO3表现了___________性和_____________ 性,毎有1 molFe参加反应转移电子______________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25 g mL-1、质量分数为36.5%的浓盐酸配制240 mL 0.1 mol L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为 。
(2)配制 240 mL 0.1 mol L-1的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(1)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30 mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30 mL), 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12 cm处
(4)若实验中遇到下列情况,对盐酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用于稀释盐酸的烧杯未洗涤, 。
②容量瓶中原有少量蒸馏水, 。
③定容时观察液面俯视, 。
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度 。
②向容量瓶中转移溶液时有滚液不慎有溶液溅出 。
③定容摇勻后发现液面下降 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水既不是氧化剂,也不是还原剂的是
A.2Na+2H20=2Na0H+H2↑ B.C12+H20=HC1+HC10
C.2F2+2H20=4HF+02 D.2H20![]() 2H2↑+02↑
2H2↑+02↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中氯离子浓度与50mL1mol·L-1的AlCl3溶液中氯离子浓度相等的是 ( )
A.150mL1mol·L-1的NaCl B.150mL3mol·L-1的KCl
C.75mL2 mol·L-1的CaCl2 D.75mL2mol·L-1的NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g H2完全燃烧生成水蒸气放出热量121 kJ,且O2中1 mol O===O键完全断裂时吸收热量496 kJ,水蒸气中形成1 mol H—O键时放出热量463 kJ,则H2中1 mol H—H键断裂时吸收的热量为( )
A. 920 kJ B. 557 kJ C. 436 kJ D. 188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1mol的CuSO45H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO45H2O受热分解的化学方程式为:CuSO45H2O(s) ![]() CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是( )
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是( )
A.△H2>△H3 B.△H1<△H3 C.△H1+△H3=△H2 D.△H1+△H2>△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中有如下反应:aX(g)+bY(g)![]() nW(g) △H,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g) △H,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
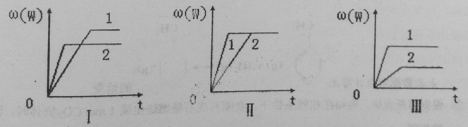
其中,ω(W)表示W在反应混合物中的体积分数,t表示反应时间。当其它条件不变时,下列分析正确的是
A.图I可能是不同压强对反应的影响,且p2>p1,a+b>n
B.图II可能是不同压强对反应的影响,且p1>p2,n<a+b
C.图II可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好
D.图III可能是不同温度对反应的影响,且T1>T2,△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com