
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 先根据n=$\frac{V}{{V}_{m}}$计算出标准状况下3.36L该气体的物质的量,然后根据M=$\frac{m}{n}$计算出该气体的摩尔质量,从而可知该气体的相对分子量,然后结合该元素的相对原子质量计算出该气体每个分子中所含原子的个数.
解答 解:标准状况时的体积3.36L该气体的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,
该气体分子的摩尔质量为:$\frac{7.2g}{0.15mol}$=48g/mol,该气体的相对分子质量为48,
已知该元素的相对原子质量是16,则该气体每个分子中所含原子的个数为:$\frac{48}{16}$=3,
故选C.
点评 本题考查了物质的量相关计算,题目难度不大,明确摩尔质量与相对分子质量之间的关系巍峨解答关键,注意熟练掌握物质的量与气体摩尔体积、摩尔质量之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
| 实验序号 | 固体质量 | 加入某浓度盐酸的体积/mL | 加入某浓度NaOH的体积/mL | 收集到气体体积/mL |
| 1 | 0.9 | 20.0 | ─ | 1008 |
| 2 | 0.9 | 30.0 | ─ | 1008 |
| 3 | 0.9 | ─ | 20.0 | 672 |
| 4 | 0.9 | ─ | 30.0 | 672 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
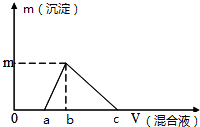 往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )
往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )| A. | a=25mL | B. | b=33mL | C. | c=100mL | D. | m=0.195g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol | B. | 0.15mol | C. | 0.1mol | D. | 0.075mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,1mol N2与足量H2混合反应生成NH3,转移电子数6NA | |
| B. | 在常温常压下,2.8g N2和CO的混合气体所含电子数为1.4NA | |
| C. | 标准状况下,22.4L CCl4含有的分子数目为NA | |
| D. | 在电解精炼粗铜的过程中,当转移电子数为NA时,阳极溶解32g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
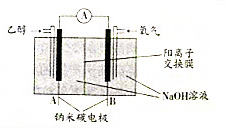
| A. | A极为电池负极,B极为电池正极 | |
| B. | B极的电极反应式为O2+2H2O+4e-═4OH- | |
| C. | 该乙醇燃料电池的总反应方程式为:C2H5OH+3O2═2CO2+3H2O | |
| D. | 当电池消耗4.6g乙醇时,经过阴离子交换膜的OH-为1.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3固体 | B. | 3 mol•L-1的H2SO4溶液 | ||
| C. | CH3COOK溶液 | D. | KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①③ | C. | ①②⑤ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com