
现有电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH,且已知:CO2+3H2O+2AlO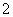 ===2Al(OH)3↓+CO
===2Al(OH)3↓+CO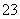 。
。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________________。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,其pH变化最大的是________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,有气体产生的是________(填编号)。
(4)将上述①②③④四种电解质溶液混合时,发生反应的离子方程式为_________________________________________________。
解析 (1)根据所给离子方程式,说明HCO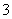 的电离程度大于Al(OH)3的酸式电离程度,故所给溶液pH相同时,其浓度由大到小的顺序为c(CH3COONa)>c(NaHCO3)>c(Na2CO3)>c(NaAlO2)>c(NaOH)。
的电离程度大于Al(OH)3的酸式电离程度,故所给溶液pH相同时,其浓度由大到小的顺序为c(CH3COONa)>c(NaHCO3)>c(Na2CO3)>c(NaAlO2)>c(NaOH)。
(2)稀释相同倍数时,由于NaOH溶液不存在水解平衡,故pH变化最大。
(3)Al3+与CO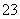 、HCO
、HCO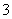 发生双水解反应,有CO2生成。
发生双水解反应,有CO2生成。
(4)①②③④四种溶液中能发生反应的只有NaHCO3和NaAlO2溶液,因电离程度HCO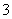 >Al(OH)3,故反应有Al(OH)3生成。
>Al(OH)3,故反应有Al(OH)3生成。
答案 (1)④②①③⑤
(2)⑤
(3)①②
(4)HCO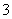 +AlO
+AlO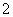 +H2O===Al(OH)3↓+CO
+H2O===Al(OH)3↓+CO


科目:高中化学 来源: 题型:
生物质能来源于植物及其加工产品所贮存的能量,是人类赖以生存的重要能源。下列有关叙述不正确的是( )
A.绿色植物通过光合作用,将化学能转化为生物质能
B.农村通过杂草和动物的粪便发酵制沼气,沼气的主要成分是甲烷
C.推广使用乙醇汽油,乙醇可由富含淀粉的农作物发酵产生
D.开发生物质能有利于环境保护和经济可持续发展
查看答案和解析>>
科目:高中化学 来源: 题型:
有两种气态烷烃的混合物,在标准状况下密度为1.16 g·L-1,则关于此混合物组成的说法正确的是( )
A.一定有乙烷
B.一定有丙烷
C.可能是乙烷和丙烷的混合物
D.可能是甲烷和丁烷的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
用已知物质的量浓度的酸测定未知物质的量浓度的碱时,会导致待测碱液的物质的量浓度偏低的操作是( )
①酸式滴定管在滴定前未将液面调至“0”刻度,而调在“2.40” ②碱式滴定管用蒸馏水洗后,未用待测液润洗
③滴定前酸式滴定管尖嘴部分未充满溶液,滴定后充满溶液 ④滴定中不慎将锥形瓶内液体摇出瓶外 ⑤滴定达终点时,视线高于滴定管内液面凹面的最低点
A.①②④ B.②③④
C.②③⑤ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.200 0 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在密闭容器中能表示反应X(g)+2Y(g)2Z(g)一定达到平衡状态的是( )
①X、Y、Z的物质的量之比为1:2:2 ②X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④
C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为32,则Y的转化率最接近于( )
A.33% B.40%
C.50% D.67%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在101 kPa时,1 mol H2完全燃烧生成气态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ·mol-1
B.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度
C.在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ·mol-1
D.在稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.31 kJ·mol-1。若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3∶2。则剩余固体的组成及物质的量之比是 ( )。
A.1∶1混合的Pb3O4、PbO
B.1∶2混合的PbO2、Pb3O4
C.1∶4∶1混合的PbO2、Pb3O4、PbO
D.1∶4∶1混合的PbO2、Pb3O4、PbO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com