
| A、过氧化钡的化学式为Ba2O2 |
| B、晶体中阴阳离子个数比为2:1 |
| C、1mol过氧化钡与足量水反应生成0.5mol氧气 |
| D、过氧化钠和过氧化钡都是强氧化剂 |
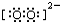 ,晶体中阴阳离子个数比为1:1,故B错误;
,晶体中阴阳离子个数比为1:1,故B错误;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 结论 |
| A | 向Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向沸水中逐滴加入1~2mL FeCl3饱和溶液,煮沸至红褐色液体 | 制备Fe(OH)3胶体 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 | 说明常温下Ksp(BaCO3) <Ksp(BaCO4) |
| D | 向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①与②混合,所得混合溶液的pH=3 |
| B、②和③混合后,溶液呈酸性 |
| C、③和④分别用②中和,消耗②的体积:③>④ |
| D、若将四种溶液稀释100倍,溶液pH大小顺序:③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温时,某溶液中由水电离出来的c(H+ )和c(OH- )的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO4 2- | ||
B、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
| ||
| C、油脂、淀粉和蛋白质在一定条件下都能发生水解反应 | ||
| D、SiO2和Al2O3都既能与酸反应,又能与碱反应,二者都属于两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯气是一种化学性质活泼的气体.
氯气是一种化学性质活泼的气体.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应是置换反应 |
| B、钾元素化合价降低 |
| C、铁元素化合价不变 |
| D、该反应是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R在元素周期表中位置为第四周期VIII族 |
| B、Na2RO4水溶液可以用于杀菌消毒和净水 |
| C、1molY或Z与足量的R反应均转移2mol电子 |
| D、G为极性分子,中心原子采取sp2杂化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com