
【题目】 (2﹣羟基﹣4﹣苯基丁酸乙酯)是某药物的中闻体,常温下是一种无色透明的油状液体,沸点为212℃.某同学设计实验制备该物质:原料:
(2﹣羟基﹣4﹣苯基丁酸乙酯)是某药物的中闻体,常温下是一种无色透明的油状液体,沸点为212℃.某同学设计实验制备该物质:原料:  (2﹣羟基﹣4﹣苯基丁酸)和乙醇 实验装置:
(2﹣羟基﹣4﹣苯基丁酸)和乙醇 实验装置:
实验步骤:
①按如图1装置连接仪器.
②20mL 2﹣羟基﹣4﹣苯基丁酸于三颈瓶中,加入适量浓硫酸和20mL无水乙醇,加入几块沸石.
③加热至70℃左右保持恒温半小时.
④分离、提纯三颈瓶中粗产品,得到有机产品.
⑤精制产品.
请回答下列问题:
(1)加入原料时,能否最先加入浓硫酸?(填“能”或“否”).油水分离器的作用是 .
(2)本实验的加热方式宜用(填“直接加热”或“水浴加热”).如果温度过高,或浓硫酸的量过多,制备产率会(填“增大”、“减小”或“不变”).
(3)写出制备反应的化学方程式: .
(4)分离提纯产品:取三颈瓶中混合物加入足量的饱和碳酸钠溶液,分液得到有机层.饱和碳酸钠溶液的作用是 . ①吸收过量的乙醇 ②除去过量的有机酸 ③促进产品水解 ④降低产品在水中溶解度
(5)产品精制:精制产品的实验装置如图2所示,试分析装置是否合理,若不合理将如何改进: . (若装置合理,此空不作答).
【答案】
(1)否;及时分离产物水,促进平衡向生成酯的反应方向移动
(2)水浴加热;减小
(3)
(4)①②④
(5)温度计的水银球要处在蒸馏烧瓶的支管口处,冷却水应从下口进上口出
【解析】解:(1)原料加入依据先加入密度小的再加入密度大的液体,所以浓硫酸应最后加入,防止浓硫酸使有机物脱水,被氧化等副反应发生,防止乙醇和酸在浓硫酸溶解过程中放热而挥发;2﹣羟基﹣4﹣苯基丁酸于三颈瓶中,加入适量浓硫酸和20mL无水乙醇发生的是酯化反应,存在化学平衡,油水分离器的作用及时分离生成的水,促进平衡正向进行分析,
所以答案是:否;及时分离产物水,促进平衡向生成酯的反应方向移动;(2)依据反应需要可知温度70°C,需要用温度计控制水浴的温度,所以加热方式是水浴加热,如果温度过高,或浓硫酸的量过多,制备产率会导致产率减小,所以答案是:水浴加热,减小;(3)2﹣羟基﹣4﹣苯基丁酸和乙醇在浓硫酸催化作用下水浴加热反应生成2﹣羟基﹣4﹣苯基丁酸乙酯和水,依据酯化反应的实质是酸脱羟基、醇脱氢,该反应的化学方程式为  ,
,
所以答案是:  ;(4)饱和碳酸钠溶液可以吸收挥发出的乙醇,中和挥发出的2﹣羟基﹣4﹣苯基丁酸,降低生成酯的溶解度;
;(4)饱和碳酸钠溶液可以吸收挥发出的乙醇,中和挥发出的2﹣羟基﹣4﹣苯基丁酸,降低生成酯的溶解度;
①乙醇易挥发,在生成物中含有乙醇易溶于水,碳酸钠溶液吸收过量的乙醇,符合碳酸钠溶液的作用,故①正确;
②有机酸在加热过程中挥发出掺入产物,加入碳酸钠溶液和酸反应可以除去过量的有机酸,故②正确;
③饱和碳酸钠溶液降低产品在水中溶解度,不是促进产品水解,故③错误;
④降低产品在水中溶解度,利于生成的酯分层分离,故④正确;
所以答案是:①②④;(5)依据蒸馏装置和原理分析判断装置图中存在的问题,分析装置图不合理,其中温度计位置错误,冷凝管水流方向错误,应使温度计处在蒸馏烧瓶的支管口处,冷却水应从下口进上口出,
所以答案是:温度计处在蒸馏烧瓶的支管口处,冷却水应从下口进上口出.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】【化学—选修5:有机化学基础】功能高分子I的一种合成路线如下,其中D能与Na反应生成H2,且D苯环上的一氯代物有2种。

已知:![]()
回答下列问题:
(1)A的名称为________,试剂a为________。
(2)C的结构简式为________。
(3)F中的官能团名称为________。
(4)上述①~⑧的反应中,不属于取代反应的是________(填数字编号)。写出反应⑦的化学方程式________。
(5)符合下列条件的B的同分异构体有________种(不考虑立体异构)。
①苯环上有氨基(—NH2) ②能发生银镜反应
其中核磁共振氢谱有4组峰,且峰面积比为2∶2∶2∶1的结构简式为________。
(6)参照上述合成路线,以1-丁烯为原料(无机试剂任选),设计制备乳酸(![]() )的合成路线________。
)的合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5时,发生以下两个分解反应:N2O5N2O3+O2 , N2O3N2O+O2 , 在1L密闭容器中加热 4mol N2O5达到化学平衡时c(O2)为4.50mol/L,c(N2O3)为1.62mol/L,则在该温度下各物质的平衡浓度正确的是( )
A.c(N2O5)=1.44 mol/L
B.c(N2O5)=0.94 mol/L
C.c(N2O)=1.40 mol/L
D.c(N2O)=3.48 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料。下列关于聚乙炔叙述错误的是( )
A. 聚乙炔是以乙炔为单体发生加聚反应形成的高聚物
B. 聚乙炔的化学式为![]() ,分子中所有碳原子在同一直线上
,分子中所有碳原子在同一直线上
C. 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质
D. 聚乙炔树脂自身不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、铁、硒、钴、磷及其化合物在工业上有重要用途,回答下列问题:
(1)铁离子(Fe3+)最外层电子排布式为______,其核外共有______种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是____________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为________(用元素符号表示)。
(3)Na3[Co(NO2)6]常用作检验K+的试剂,Na3[Co(NO2)6]中存在的化学键有__________。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如下左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为______,其中心原子杂化轨道类型为__________,B为________。
(5)磷化铝晶胞如图所示,A1原子的配位数为________,若两个铝原子之间的最近距离为d pm,NA代表阿伏加德罗常数的值, 则磷化铝晶体的密度ρ=_________g/cm3。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车发动机在工作时,由于电喷,在气缸中会发生反应:N2(g)+O2(g)=2NO(g)。已知该反应过程中的能量变化如图所示,下列说法中错误的是( )
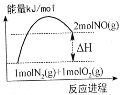
A. 该反应过程中有共价键的断裂和形成
B. 该反应是氧化还原反应
C. 该反应是放热反应
D. 使用催化剂可以改变反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯和苯属于不同类型的有机化合物,但它们之间也有共性。下列关于它们之间共同特点的说法正确的有
A. 都由C和H两种元素组成 B. 都能使酸性KMnO4溶液褪色
C. 都能发生加成反应和取代反应 D. 在氧气中完全燃烧后都生成CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍具有较高的经济价值。工业上采用一定方法处理含镍废水使其达标排放并回收镍。某电镀废水中的镍主要以NiRz络合物形式存在,在水溶液中存在以下平衡: NiR2(aq) ![]() Ni2+(aq) +2R-(aq) (R-为有机物配体,K=1.6×10-14)
Ni2+(aq) +2R-(aq) (R-为有机物配体,K=1.6×10-14)
(1)传统的“硫化物沉淀法”是向废水中加入Na2S,使其中的NiR2 生成NiS 沉淀进而回收镍。
①该反应的离子方程式为_______________。
②NiS 沉淀生成的同时会有少量Ni(OH)2沉淀生成,用离子方程式解释Ni(OH)2生成的原因是______________。
(2)“硫化物沉淀法”镍的回收率不高,处理后废水中的镍含量难以达标。“铁脱络-化学沉淀法”可达到预期效果,该法将镍转化为Ni(OH)2固体进而回收镍。工艺流程如下:

“脱络”(指镍元素由络合物NiR2转化成游离的Ni3+) 过程中,R-与中间产物-OH (羟基自由基) 反应生成难以与Ni2+络合的-R (有机物自由基),但-OH也能与H2O2发生反应。反应的方程式如下:Fe2+ + H2O2 = Fe3+ +OH-+-OH i
R- +-OH =OH-+-R ii
H2O2+2-OH=O2↑+ 2H2O iii
实验测得“脱络”过程中H2O2的加入量对溶液中镍去除率的影响如图所示:

①从平衡移动的角度解释加入Fe2+和H2O2能够实现“脱络”的原因是______________。
②分析图中曲线,可推断过氧化氢的最佳加入量为_______________ g/ L; 低于或高于这个值,废水处理效果都下降,原因是____________。
(3) 工业上还可用电解法制取三氧化二镍。①用NaOH溶液调节NiCl2溶液PH至7.5,加入适量硫酸钠后采用情性电极进行电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。写出ClO- 氧化Ni (OH) 2生成三氧化二镍的离子方程式是______, amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量是_________。
②电解法制取三氧化二镍实际过程中,有时获得一种结晶水合物,已知1mol 该物质中含有0.5mol结晶水。取该化合物20.2g进行充分加热,而获得三氧化二镍固体和0.2mol水,则该结晶水合物的化学式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com