
| A£® | ÓÉH+£Øaq£©+OH- £Øaq£©=H2O£Øl£©”÷H=-57.3 kJ•mol-1£ŗæÉÖŖŗ¬1 molĒāŃõ»Æ±µµÄČÜŅŗÓėŗ¬0.5 molĮņĖįµÄĻ”ČÜŅŗ»ģŗĻ£¬·Å³öČČĮæ“óÓŚ57.3 kJ | |
| B£® | ÓÉH2O£Øg£©=H2O£Øl£©”÷H=-44.0kJ•mol-1æÉÖŖŹĒ·ÅČČ·“Ó¦£» | |
| C£® | ÓÉSO2£Øg£©+$\frac{1}{2}$O2£Øg£©?SO3£Øg£©”÷H=-98.3 kJ•mol-1æÉÖŖ£¬ŌŚĆܱÕČŻĘ÷ÖŠ³äČė2 mol SO2ŗĶ1 mol O2³ä·Ö·“Ó¦ŗ󣬷ųöČČĮæĪŖ196.6 kJ | |
| D£® | ĒāĘųµÄČ¼ÉÕČČ£Ø”÷H£©ĪŖ-285.5kJ/mo1£¬ŌņĖ®µē½āµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2H2O£Ø1£©=2H2£Øg£©+O2£Øg£©”÷H=+285.5KJ/mo1 |
·ÖĪö A£®ĒāŃõ»Æ±µŗĶĮņĖį·“Ӧɜ³ÉĖ®µÄĶ¬Ź±Éś³ÉĮņĖį±µ³Įµķ£»
B£®H2O£Øg£©=H2O£Øl£©ĪŖĪļĄķ±ä»Æ£»
C£®ĪŖæÉÄę·“Ó¦£»
D£®ĪüŹÕČČĮæŹżÖµ“ķĪó£®
½ā“š ½ā£ŗA£®ĮņĖįøłÓė±µĄė×Ó·“Ӧɜ³ÉĮņĖį±µ³ĮµķŅ²»į·ÅČČ£¬ĖłŅŌ·Å³öČČĮæ“óÓŚ57.3 kJ£¬¹ŹAÕżČ·£»
B£®H2O£Øg£©=H2O£Øl£©ĪŖĪļĄķ±ä»Æ£¬¶ųĪüČČ·“Ó¦”¢·ÅČČ·“Ó¦Ö»Õė¶Ō»Æѧ±ä»Æ£¬¹ŹB“ķĪó£»
C£®·“Ó¦ĪŖæÉÄę·“Ó¦£¬2 mol SO2ŗĶ1 mol O2²»æÉÄÜĶźČ«·“Ó¦£¬·Å³öČČĮæÉŁÓŚ196.6 kJ£¬¹ŹC“ķĪó£»
D£®ĒāĘųµÄČ¼ÉÕČČ£Ø”÷H£©ĪŖ-285.5kJ/mo1£¬ŌņĖ®µē½āµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2H2O£Ø1£©=2H2£Øg£©+O2£Øg£©”÷H=+571KJ/mo1£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²é»Æѧ·“Ó¦ÓėÄÜĮæ±ä»Æ£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŅŌ¼°Ė«»łµÄ漲飬עŅā°ŃĪÕÖŠŗĶČČ”¢·“Ó¦ČȵČĻą¹ŲøÅÄīŅŌ¼°æÉÄę·“Ó¦µÄĢŲµć£¬ĪŖŅדķµć£¬ÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö“ó·“Ó¦ĪļµÄÅØ¶Č£¬Ę½ŗā³£ŹżKŌö“ó | B£® | ¼Ó“óĢåĻµŃ¹Ēæ£¬Ę½ŗā³£ŹżKŌö“ó | ||
| C£® | ¼ÓČėøŗ“߻ƼĮ£¬Ę½ŗā³£ŹżK¼õŠ” | D£® | ÉżøßĪĀ¶Č£¬Ę½ŗā³£ŹżK·¢Éś±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
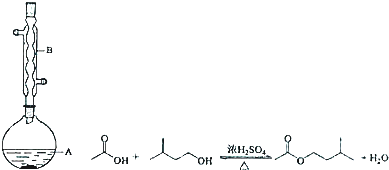
| Ļą¶Ō·Ö×ÓÖŹĮæ | ĆܶČ/£Øg•cm-3£© | ·Šµć/”ę | Ė®ÖŠČܽāŠŌ | |
| ŅģŹł“¼ | 88 | 0.8123 | 131 | Ī¢ČÜ |
| ŅŅĖį | 60 | 1.0492 | 118 | ČÜ |
| ŅŅĖįŅģĪģõ„ | 130 | 0.8670 | 142 | ÄŃČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
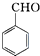 +KOH”ś
+KOH”ś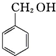 +
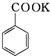
+
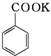 +HCl”ś
+HCl”ś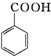 +KCl
+KCl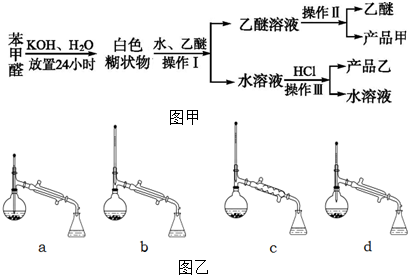
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃé·½°øÓė²½Öč | ŹµŃéĻÖĻóŗĶ½įĀŪ |
| 1£®½«ÉŁĮæĘųĢåĶØČėŹ¢ÓŠÉŁĮæĘ·ŗģČÜŅŗµÄŹŌ¹ÜÄŚ£» | ČōĘ·ŗģČÜŅŗĶŹÉ«£¬ŌņĪŽÉ«ĘųĢåÖŠÓŠSO2£® |
| 2£®½«ĘųĢåĶعż×°ÓŠ×ćĮæĒāŃõ»ÆÄĘČÜŅŗµÄĻ“ĘųĘæŗó£¬ÓĆŠ”ŹŌ¹ÜŹÕ¼ÆĘųĢ壬²¢ŌŚ¾Ę¾«µĘÉĻµćČ¼ | ČōŹÕ¼Æµ½ĘųĢåæÉŅŌČ¼ÉÕ£¬ŌņĪŽÉ«ĘųĢåÖŠÓŠH2£® ½įŗĻŅŌÉĻŹµŃéæÉÖŖ¼ŁÉčČż³ÉĮ¢£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »Æѧ·“Ó¦¶¼°éĖę×ÅČČĮæµÄ±ä»Æ | |
| B£® | øö±š»Æѧ·“Ó¦ÓėÄÜĮæ±ä»ÆĪŽ¹Ų | |
| C£® | ijŠ©ĪüČČ·“Ó¦ŌŚ²»¼ÓČČĢõ¼žĻĀŅ²ÄÜ·¢Éś | |
| D£® | ·ÅČČ·“Ó¦µÄ·¢ÉśĪŽŠčČĪŗĪĢõ¼ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| »Æѧ¼ü | H-Cl | OØTO | Cl-Cl | H-O |
| E/£ØkJ•mol-1£© | 431 | 397 | a | 465 |
| A£® | 242 | B£® | 303.5 | C£® | 180.5 | D£® | 365 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 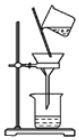 ³żČ„“ÖŃĪČÜŅŗÖŠ²»ČÜĪļ | B£® |  Ģ¼ĖįĒāÄĘŹÜČČ·Ö½ā | ||
| C£® | 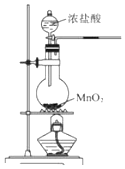 ÖĘȔɣĮæCl2 | D£® | 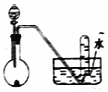 Ļ”ĻõĖįÓėĶµÄ·“Ó¦ÖĘČ”²¢ŹÕ¼ÆNO |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com