
分析 (1)原子的最外层电子数与共价键的数目相同时,所有的价电子都参与形成共价键;
(2)只有一个价电子参与形成共价键,则分子中只有一个共价键;
(3)最外层有未参与成键的电子对,则最外层电子数大于共价键数;
(4)单键中只有σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和2个π键.
解答 解:(1)原子的最外层电子数与共价键的数目相同时,所有的价电子都参与形成共价键,H2O和C2H6中所有的价电子都参与形成共价键;
故答案为:BE;
(2)只有一个价电子参与形成共价键,则分子中只有一个共价键,HCl中只含有一个H-Cl键,故答案为:C;
(3)最外层有未参与成键的电子对,则最外层电子数大于共价键数,NH3 中N原子含有一个孤对电子,H2O中O原子含有2个孤电子对,HCl中Cl含有3个孤电子对,N2
中每个N原子含有一个孤电子对;
故答案为:ABCF;
(4)单键中只有σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和2个π键,N2的结构式为N≡N,分子中含有一个三键,则既有σ键,又有π键,
故答案为:F.
点评 本题考查了共价键的类型、共用电子对的判断,题目难度不大,侧重于基础知识的考查,注意把握共用电子对与共价键的关系.


科目:高中化学 来源: 题型:选择题
| A. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| B. | CH2=CH(CH3)C=CH2 2-甲基-1,3-二丁烯 | |
| C. | CH2(OH)CH2CH2CH2OH 1,4-二羟基丁醇 | |
| D. | CH3CH2CHClCCl2CH3 2,2,3-三氯戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ca2+、OH-、HCO3- | B. | Ag+、H+、SO32-、ClO- | ||
| C. | NH4+、Br-、Na+、SO42- | D. | H+、Cl-、Fe2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 盐桥中的电解质可以用KC1 | |
| B. | 闭合K,外电路电流方向为Fe电极→石墨电极 | |
| C. | 闭合K,石墨电极上只生成铜 | |
| D. | 导线中流过0.15 mol e-时,加入5.55 gCu2(OH)2CO3,CuSO4溶液可恢复原组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难溶电解质的溶解平衡是一种动态平衡 | |
| B. | 达到溶解平衡时,沉淀的速率和溶解的速率相等,溶液中离子的浓度保持不变 | |
| C. | 达到溶解平衡时,溶液中各种离子的浓度不一定相等 | |
| D. | 达到溶解平衡时,再加入该难溶电解质,将促进其溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率 | |
| B. | 对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 | |
| C. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 | |
| D. | 100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 10 | C. | 4 | D. | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: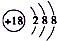 | B. | 四氯化碳分子的比例模型: | ||
| C. | 次氯酸的电子式: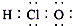 | D. | 中子数为16的硫离子:${\;}_{16}^{32}$S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com