
 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Cl2��Fe3+��I2��SO2 | B��Cl2 ��I2��Fe3+��SO2 |
| C��Cl2��Fe3+��SO2��I2 | D��Fe3+��I2��Cl2 ��SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �������ĵ缫��ӦΪ��M��2e����M2+ ��Y��������ϡH2SO4�У�M����ϡH2SO4�����������ֽ����Ļ��������ǿ��˳���ǣ�
�������ĵ缫��ӦΪ��M��2e����M2+ ��Y��������ϡH2SO4�У�M����ϡH2SO4�����������ֽ����Ļ��������ǿ��˳���ǣ�| A��M<N<Y<X<Z | B��N<M<X<Y<Z | C��N<M<Y<X<Z | D��X<Z<N<M<Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��MnO2+4HCl��Ũ�� MnCl2+Cl2��+2H2O |
| B��K2Cr2O7+6FeSO4+7H2SO4��Cr2��SO4��3+3Fe2��SO4��3+K2SO4��7H2O |
| C��2Al+2NaOH+2H2O=2NaAlO2+3H2�� |
| D��2KMnO4+HCOOK+KOH=2K2MnO4+CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na | B��NO2 | C��Fe2+ | D��H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HCl�������Ժͻ�ԭ�� |
| B������1mol Cl2ʱ��ת��10mol���� |
| C��HCl���ֱ�������������HClռ�μӷ�ӦHCl��5/8 |
| D����������ʽ˵����ԭ�ԣ�KMnO4>Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ����������Fe2(SO4)3��Һ��ȫ��Ӧ���ټ���K2Cr2O7��Һ����������������ѧ��Ӧ��SO2��2Fe3����2H2O===SO
����������Fe2(SO4)3��Һ��ȫ��Ӧ���ټ���K2Cr2O7��Һ����������������ѧ��Ӧ��SO2��2Fe3����2H2O===SO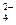 ��4H����2Fe2����
��4H����2Fe2����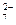 ��6Fe2����14H��===2Cr3����6Fe3����7H2O��
��6Fe2����14H��===2Cr3����6Fe3����7H2O��| A����ԭ�ԣ�Cr3��>Fe2��>SO2 | B�������ԣ�Cr2O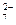 >SO2>Fe3�� >SO2>Fe3�� |
C��Cr2O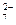 �ܽ�Na2SO3������Na2SO4 �ܽ�Na2SO3������Na2SO4 | D��������Ӧ��Fe2(SO4)3������ԭ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com