
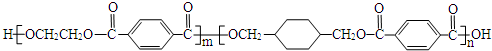
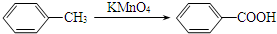
 £®
£® £®
£® ·ÖĪö øł¾ŻPETGµÄ½į¹¹¼ņŹ½æÉŅŌ擳öPETGŹĒÓÉ ”¢HOCH2CH2OH”¢
”¢HOCH2CH2OH”¢ ČżÖÖµ„ĢåĶعżĖõ¾Ū·“Ó¦µĆµ½µÄŅ»ÖÖøß¾ŪĪļ£»PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬øł¾ŻRCOOR1+R2OH”śRCOOR2+R1OHÖŖ£¬DŗĶHŹĒ“¼£¬ŌņEŹĒ
ČżÖÖµ„ĢåĶعżĖõ¾Ū·“Ó¦µĆµ½µÄŅ»ÖÖøß¾ŪĪļ£»PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬øł¾ŻRCOOR1+R2OH”śRCOOR2+R1OHÖŖ£¬DŗĶHŹĒ“¼£¬ŌņEŹĒ £¬BŗĶøßĆĢĖį¼Ų·“Ӧɜ³É
£¬BŗĶøßĆĢĖį¼Ų·“Ӧɜ³É £¬ŌņBŹĒ
£¬ŌņBŹĒ £¬BŗĶĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ
£¬BŗĶĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ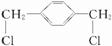 £¬F·¢ÉśĖ®½ā·“Ӧɜ³ÉGĪŖ
£¬F·¢ÉśĖ®½ā·“Ӧɜ³ÉGĪŖ £¬GÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHŹĒ
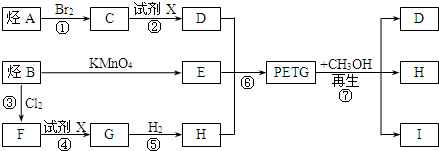
£¬GÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHŹĒ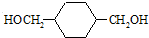 £®DŹĒŅŅ¶ž“¼£¬ŌņAŹĒŅŅĻ©£¬ŅŅĻ©ŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ1”¢2¶žäåŅŅĶ飬PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬½įŗĻĢāøųŠÅĻ¢ÖŖ£¬IŹĒ
£®DŹĒŅŅ¶ž“¼£¬ŌņAŹĒŅŅĻ©£¬ŅŅĻ©ŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ1”¢2¶žäåŅŅĶ飬PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬½įŗĻĢāøųŠÅĻ¢ÖŖ£¬IŹĒ £®
£®
½ā“š ½ā£ŗøł¾ŻPETGµÄ½į¹¹¼ņŹ½æÉŅŌ擳öPETGŹĒÓÉ ”¢HOCH2CH2OH”¢
”¢HOCH2CH2OH”¢ ČżÖÖµ„ĢåĶعżĖõ¾Ū·“Ó¦µĆµ½µÄŅ»ÖÖøß¾ŪĪļ£»PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬øł¾ŻRCOOR1+R2OH”śRCOOR2+R1OHÖŖ£¬DŗĶHŹĒ“¼£¬ŌņEŹĒ
ČżÖÖµ„ĢåĶعżĖõ¾Ū·“Ó¦µĆµ½µÄŅ»ÖÖøß¾ŪĪļ£»PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬øł¾ŻRCOOR1+R2OH”śRCOOR2+R1OHÖŖ£¬DŗĶHŹĒ“¼£¬ŌņEŹĒ £¬BŗĶøßĆĢĖį¼Ų·“Ӧɜ³É
£¬BŗĶøßĆĢĖį¼Ų·“Ӧɜ³É £¬ŌņBŹĒ
£¬ŌņBŹĒ £¬BŗĶĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ
£¬BŗĶĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉFĪŖ £¬F·¢ÉśĖ®½ā·“Ӧɜ³ÉGĪŖ
£¬F·¢ÉśĖ®½ā·“Ӧɜ³ÉGĪŖ £¬GÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHŹĒ
£¬GÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHŹĒ £®DŹĒŅŅ¶ž“¼£¬ŌņAŹĒŅŅĻ©£¬ŅŅĻ©ŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ1”¢2¶žäåŅŅĶ飬PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬½įŗĻĢāøųŠÅĻ¢ÖŖ£¬IŹĒ
£®DŹĒŅŅ¶ž“¼£¬ŌņAŹĒŅŅĻ©£¬ŅŅĻ©ŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉCĪŖ1”¢2¶žäåŅŅĶ飬PETGŗĶ¼×“¼·“Ӧɜ³ÉD”¢IŗĶH£¬½įŗĻĢāøųŠÅĻ¢ÖŖ£¬IŹĒ £®
£®
£Ø1£©·“Ó¦¢ßŹōÓŚČ”“ś·“Ó¦£¬Ā±“śĢžŌŚĒāŃõ»ÆÄʵÄĖ®ČÜŅŗÖŠÄÜÉś³É“¼£¬ĖłŅŌXŹĒNaOHČÜŅŗ£¬
¹Ź“š°øĪŖ£ŗČ”“ś·“Ó¦£»ĒāŃõ»ÆÄĘČÜŅŗ£»
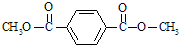
£Ø2£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬IµÄ½į¹¹¼ņŹ½·Ö±šĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ÓɾŪŗĻĪļæÉÖŖ£¬ŗĻ³ÉŹ±Ó¦æŲÖʵĵ„ĢåµÄĪļÖŹµÄĮæ£ŗn£ØD£©£ŗn£ØE£©£ŗn£ØH£©=m£ŗ£Øm+n£©£ŗn£¬
¹Ź“š°øĪŖ£ŗm£ŗ£Øm+n£©£ŗn£»
£Ø4£©·“Ó¦¢ŚŹĒĀ±“śĢž·¢ÉśµÄĖ®½ā·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗBrCH2CH2Br+2NaOH$”ś_{”÷}^{Ė®}$HOCH2CH2OH+2NaBr£¬
¹Ź“š°øĪŖ£ŗBrCH2CH2Br+2NaOH$”ś_{”÷}^{Ė®}$HOCH2CH2OH+2NaBr£»
£Ø5£©EµÄ½į¹¹¼ņŹ½ĪŖ £¬EµÄĶ¬·ÖŅģ¹¹Ģå·ūŗĻ£ŗ¢ŁÄÜÓėNaHCO3ČÜŅŗ·“Ӧɜ³ÉCO2 £¬ĖµĆ÷ŗ¬ÓŠ-COOH£¬¢ŚÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ŗ¬ÓŠČ©»ł£¬¢ŪÓöFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ŗ¬ÓŠ·ÓōĒ»ł£¬¼“ŗ¬ÓŠ-COOH”¢-CHO”¢-OH£¬µ±-COOH”¢-CHO“¦ÓŚĮŚĪ»Ź±£¬-OHÓŠ4ÖÖĪ»ÖĆ£¬µ±-COOH”¢-CHO“¦ÓŚ¼äĪ»Ź±£¬-OHÓŠ4ÖÖĪ»ÖĆ£¬µ±-COOH”¢-CHO“¦ÓŚ¶ŌĪ»Ź±£¬-OHÓŠ2ÖÖĪ»ÖĆ£¬¹²ÓŠ10ÖÖ£¬
£¬EµÄĶ¬·ÖŅģ¹¹Ģå·ūŗĻ£ŗ¢ŁÄÜÓėNaHCO3ČÜŅŗ·“Ӧɜ³ÉCO2 £¬ĖµĆ÷ŗ¬ÓŠ-COOH£¬¢ŚÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ŗ¬ÓŠČ©»ł£¬¢ŪÓöFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ŗ¬ÓŠ·ÓōĒ»ł£¬¼“ŗ¬ÓŠ-COOH”¢-CHO”¢-OH£¬µ±-COOH”¢-CHO“¦ÓŚĮŚĪ»Ź±£¬-OHÓŠ4ÖÖĪ»ÖĆ£¬µ±-COOH”¢-CHO“¦ÓŚ¼äĪ»Ź±£¬-OHÓŠ4ÖÖĪ»ÖĆ£¬µ±-COOH”¢-CHO“¦ÓŚ¶ŌĪ»Ź±£¬-OHÓŠ2ÖÖĪ»ÖĆ£¬¹²ÓŠ10ÖÖ£¬
¹Ź“š°øĪŖ£ŗ10£»
£Ø6£©DŗĶEŌŚ“߻ƼĮ×÷ÓĆĻĀæÉÉś²śŅ»ÖÖ¾Ūõ„ĻĖĪ¬--µÓĀŚ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻÓėŗĻ³É£¬øł¾ŻPETGµÄ½į¹¹ÅŠ¶ĻĘ䵄Ģ壬ŌŁ½įŗĻ×Ŗ»Æ¹ŲĻµ½ųŠŠĶʶĻ£¬½ĻŗƵÄæ¼²éѧɜ¶ŌŠÅĻ¢µÄ½ÓŹÜŗĶÖŖŹ¶ĒØŅĘŌĖÓĆĮ¦£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ž | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ū¢Ż | D£® | ¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | c£ØNH4+£©£¾c£ØCl-£©£¾c£ØOH-£©£¾c£Ø H+£© | B£® | c£ØCl-£©£¾c£ØNH4+£©£¾c£Ø H+£©£¾c£ØOH-£© | ||
| C£® | c£ØNH4+£©+c£Ø NH3£©=c£ØCl-£©+c£ØOH-£© | D£® | c£ØNH4+£©+c£Ø NH3•H2O£©+c£Ø NH3£©=c£ØCl-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
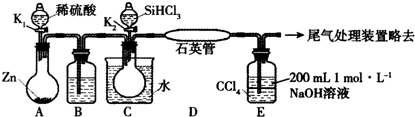
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ČÜŅŗÖŠµÄ»Æѧ·“Ó¦“󶹏ĒĄė×Ó·“Ó¦£®øł¾ŻŅŖĒó»Ų“šĻĀĮŠĪŹĢā£®
ČÜŅŗÖŠµÄ»Æѧ·“Ó¦“󶹏ĒĄė×Ó·“Ó¦£®øł¾ŻŅŖĒó»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 65gŠæÓė×ćĮæĻ”ĮņĖį·“Ó¦²śÉśµÄĘųĢåĢå»żĪŖ22.4L | |
| B£® | ±ź×¼×“æöĻĀ£¬ŅŌČĪŅā±Č»ģŗĻµÄH2ŗĶCOĘųĢå¹²8.96L£¬ŌŚ×ćĮæŃõĘųÖŠ³ä·ÖČ¼ÉÕŹ±ĻūŗÄŃõĘųµÄ·Ö×ÓŹżĪŖ0.2NA | |
| C£® | 0.2mol H2O2ŌŚMnO2“ß»ÆĻĀ³ä·Ö·“Ӧɜ³ÉO2µÄŹżÄæĪŖ0.2NA | |
| D£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬1mol H2ŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕ£¬ĻūŗÄO2µÄĢå»żĪŖ22.4L |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com