
|
CuO、Cu2O的混合物中含Cu 88%,则混合物中含CuO和Cu2O的物质的量之比为 | |
A. |
1∶5 |
B. |
3∶2 |
C. |
1∶4 |
D. |
5∶1 |
科目:高中化学 来源: 题型:
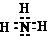
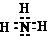
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
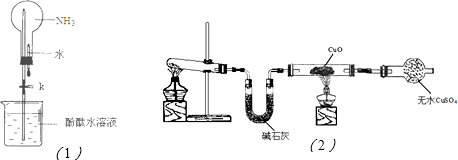
| ||
| ||
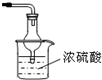 ;
; ;
;| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:江西省白鹭洲中学2012届高三上学期期中考试化学试题 题型:058
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设:
假设1:红色粉末是Fe2O3,
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3,和Cu2O的混合物
设计探究实验:
取少量粉末放人足量稀硫酸中,在所得溶液中再滴加KSCN试剂.
(1)若假设l成立,则实验现象是________.
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?________,简述你的理由(不需写出反应的方程式)________.
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是________.
探究延伸:
经实验分析,确定红色粉末为Fe2O3,和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为________.
查看答案和解析>>
科目:高中化学 来源:江西省期中题 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com