
| 39.2g |
| 98g/mol |
| n |
| V |
| 39.2g |
| 98g/mol |
|
| 0.6mol |
| (5-2) |
| 1.2mol |
| 0.5L |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
| A、金属钠保存在无水乙醇中 |
| B、冷的浓H2SO4存放于敞口铝制容器中 |
| C、少量的白磷保存在二硫化碳中 |
| D、氯气液化后贮存于钢瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中有晶体析出,Na+数目不变 |
| B、溶液中有气体逸出,Na+数目增加 |
| C、溶质的质量分数增大 |
| D、溶液中Na+数目减少,溶质质量分数未变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | 实验结论 | 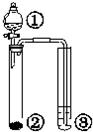 | |
| A | 稀醋酸 | CaCO3 | 澄清石灰水 | 酸性:醋酸>碳酸 | |
| B | 硫酸 | Na2SO3 | 溴水 | SO2具有还原性 | |
| C | 浓盐酸 | KMnO4 | 淀粉KI溶液 | 氧化性:KMnO4>Cl2>I2 | |
| D | 盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1);△H=-57.3 kJ/mol | ||||
B、KOH(aq)+
| ||||
C、C8H18(l)+
| ||||
| D、2C8H18(g)+25O2(g)=16CO2(g)+18 H2O(1);△H=-5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、至少存在4种离子 |
| B、Cl-一定存在,且c(Cl-)≥0.4mol/L |
| C、SO42-、NH4+一定存在 |
| D、CO32-、Al3+、K+一定不存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、250 mL、13.6 g |
| B、500 mL、5.6 g |
| C、125 mL、10.2 g |
| D、1000 mL、7.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应Ⅰ:若p1<p2,则a+b<c |
| B、反应Ⅱ:此反应的△H<0,且T1<T2 |
| C、反应Ⅲ:△H>0且T2>T1或△H<0且T2<T1 |
| D、反应Ⅳ:T1<T2,则该反应不易自发进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com