
某液态化合物X2Y4,常用作火箭燃料。32g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g) X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为22.4 L,其密度为1.25 g·L-1,则:
X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为22.4 L,其密度为1.25 g·L-1,则:
(1)反应前O2在标准状况的体积 V(O2)约为________L;
V(O2)约为________L;
(2)X2的摩尔质量为________________,Y元素的名称是______________;
(3)若反应生成0.1 mol X2,则生成Y2O的质量为________g。
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2016-2017学年甘肃省高一上期中化学试卷(解析版) 题型:选择题
为了除去硝酸钾晶体中所含的硝酸钙和硫酸镁,先将它配成溶液,然后加入几种试剂,配以过滤、蒸发结晶等操作,制成纯净的硝酸钾晶体,其加入试剂及顺序正确的是( )
A.NaOH——Na2CO3——BaCl2 ——HCl
B.NaOH——BaCl2 ——Na 2CO3——HCl
2CO3——HCl
C.KOH ——K2CO3——Ba(NO3)2——HNO3
D.KOH——Ba(NO3)2——K2CO3——HNO3
查看答案和解析>>
科目:高中化学 来源:2017届广西省柳州市高三10月模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.100℃时,某溶液pH=6,则该溶液一定显酸性
B.25℃时,0.1mol/L的NaHSO3溶液pH=4,溶液中c(SO32-)<c(H2SO3)
C.25℃时,pH=3的硫酸溶液与pH=11的氨水等体积混合,所得溶液呈酸性
D.室温下,10mL0.1mol/L CH3COOH溶液与5mL0.1mol/LNaOH溶液混合,所得溶液中有:
2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市等六校高三第一次联考化学试卷(解析版) 题型:选择题
镁—次氯酸盐燃料电池的工作原理如右图所示,该电池反应为:
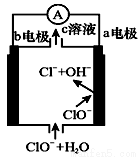
Mg+ClO-+H2O=Mg(OH)2+Cl-
下列有关说法正确的是( )
A.电池工作时,c溶液中的溶质是MgCl2
B.负极反应式:ClO--2e-+H2O=Cl-+2OH-
C.电池工作时,OH-向b电极移动
D.b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl-
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市等六校高三第一次联考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.25℃、101 kPa时,0.1NA个H2分子完全燃烧生成气态水,放出a kJ热量,表示氢气燃烧热的热化学方程式为H2(g)+ O2(g)= H2O(g) ΔH=-10a kJ·mol-1
O2(g)= H2O(g) ΔH=-10a kJ·mol-1
B.500℃、30 MPa下,N2(g)+3H2(g) 2NH3(g) ΔH=-38.6kJ·mol-1。将分子数为1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3 kJ
2NH3(g) ΔH=-38.6kJ·mol-1。将分子数为1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3 kJ
C.在反应KClO3 +6HCl = KCl+3Cl2↑+3H2O中,每生成3 mol Cl2转移的电子数为5NA
D.以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子,则正极生成的H2在标准状况下体积为22.4 L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入b mol硝酸银的溶液,恰好使氯离子完全沉淀,则该混合溶液中钾离子浓度为
A.0.1(b-2a) mol/L
B.10(2a-b) mol/L
C.10(b-a) mol/L
D.10(b-2a) mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
某硝酸钠固体中混有少量硫酸铵和硫酸镁杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。(已知NH4++OH- 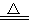 NH3↑+H2O)
NH3↑+H2O)
选择试剂 | ① | Na2CO3溶液 | ② |
实验操作 | ③ | ④ | 调节pH |
下列试剂或操作不合理的是
A.试剂①为Ba(OH)2溶液 B.试剂②为稀HNO3
C.操作③为结晶 D.操作为④过滤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上期中化学卷(解析版) 题型:填空题
按要求填空。
(1)浓度均为0.1 mol/L的①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是 (填序号)。
(2)Fe2(SO4)3溶液显酸性,用离子方程式表示其原因___________________。
(3)AlCl3溶液和NaAlO2溶液混合的化学方程式为______________________。
(4)向饱和FeCl3溶液中加入CaCO3粉末,发现碳酸钙逐渐溶解,同时还产生的现象有____________________。
(5)常温下,将0.2 mol/L CH3COOH和0.1 mol/L NaOH溶液等体积混合,所得溶液的pH<7,该混合溶液中离子浓度由大到小的顺序是_____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.1 L一氧化碳气体一定比1 L氧气的质量小
C.28 g N2和CO的混合气体在标准状况下的体积约为22.4 L
D.常温常压下,1 mol碳完全燃烧消耗22.4 L氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com