
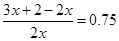 £¬½āµĆx£½4£¬¼“Aµ„ÖŹµÄŅ»øö·Ö×ÓÖŠÓŠ4øöŌ×Ó£¬·“Ó¦µÄ·½³ĢŹ½ŹĒ4AH3 = A4+6H2”£
£¬½āµĆx£½4£¬¼“Aµ„ÖŹµÄŅ»øö·Ö×ÓÖŠÓŠ4øöŌ×Ó£¬·“Ó¦µÄ·½³ĢŹ½ŹĒ4AH3 = A4+6H2”£


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ķس£×“æöĻĀµÄĘųĢåĦ¶ūĢå»żŌ¼ĪŖ22.4L |
| B£®±ź×¼×“æöĻĀµÄĘųĢåĦ¶ūĢå»żŌ¼ĪŖ22.4L |
| C£®ĻąĶ¬ĪļÖŹµÄĮæµÄĘųĢåĦ¶ūĢå»żŅ²ĻąĶ¬ |
| D£®Ä³×“æöĻĀ£¬µ„Ī»ĪļÖŹµÄĮæµÄĘųĢåĖłÕ¼µÄĢå»ż¾ĶŹĒøĆĘųĢåŌŚ“ĖדæöĻĀµÄĦ¶ūĢå»ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®150 mL 1 mol”¤L-1µÄNaCl | B£®75 mL 1 mol”¤L-1µÄFeCl2 |
| C£®150 mL 3 mol”¤L-1µÄKCl | D£®75 mL 2 mol”¤L-1µÄCaCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®29”Ć8”Ć13 | B£®22”Ć1”Ć14 | C£®13”Ć8”Ć29 | D£®29”Ć16”Ć57 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®980 ml £¬114.7g | B£®500ml, 58.5g |
| C£®1000 ml£¬ 117 g | D£®1000ml, 117.0g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®l mol N2µÄÖŹĮæĪŖ28 g/mol |
| B£®OH?µÄĦ¶ūÖŹĮæĪŖ17 g/mol |
| C£®H2SO4µÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ98 g |
| D£®l molČĪŗĪĪļÖŹµÄÖŹĮæµČÓŚøĆĪļÖŹµÄĻą¶Ō·Ö×ÓÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®11.2L | B£®33.6L”””””””” | C£®22.4L | D£®44.8L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®m/9 | B£®9m | C£®2m | D£®m |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ģ¼ĖįÄĘ | B£®ĀČ»ÆĆ¾ | C£®ĀČ»ÆÄĘ | D£®ĀČ»ÆĢś |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com