
【题目】分子式为C4H10O并能被氧化生成醛类的有机化合物有( )
A.2种
B.3种
C.4种
D.5种
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为Fe2O3(s)+CO(g)Fe(s)+CO2(g) 已知该反应在不同温度下的平衡常数如右表所示:
温度/℃ | 1 000 | 1 150 | 1 300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= , △H(填“>”“<”或“=”)0.
(2)在一个容积为10L的密闭容器中,1 000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=、CO的平衡转化率= .
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.减少Fe的量
B.加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
(4)1000℃时,某时刻CO2和CO的物质的量浓度分别为0.2molL﹣1和0.1molL﹣1 , 则此时反应是否达到平衡(填“是”或“否”),V(正)V(逆)(填“>”“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应),请回答下列问题:
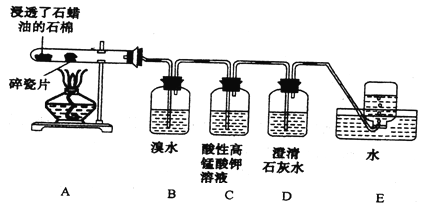
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。
例如,石油分馏产物之一的十六烧烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为______,乙的结构简式为________。
4乙,则甲的分子式为______,乙的结构简式为________。
(2)B装置中的实验现象可能是______,写出反应的化学方程式:______ , 其反应类型是_________。
(3)C装置中可观察到的现象是_______,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_______ (填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由:_________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是______(选填字母,下同);除去甲烷中乙烯的方法是_______。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是 ( ) 
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢
D.用碳酸钙(块状)与稀硫酸制二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A.K+、HCO3﹣、CO32﹣、Br﹣
B.CO32﹣、HCO3﹣、OH﹣、K+
C.K+、Ca2+、NO3﹣、CO32﹣
D.H+、Cl﹣、Na+、SO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2的分解为例,研究浓度、催化剂、溶液的酸碱性对反应速率的影响。在常温下按照如下方案设计实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
(1)实验①和②的目的是_________________________________。实验时由于没有观察到明显现象而无法得出结论。为了达到实验目的,你对原实验方案的改进措施是______________________________________________。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图所示。
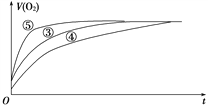
分析上图能够得出的实验结论是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在科学史上中国有许多重大的发明和发现,为世界现代物质文明奠定了基础。以下属于化学史上中国对世界重大贡献的是
①造纸 ②发现元素周期律 ③提出原子—分子论学说 ④指南针
⑤炼铜、炼铁、炼钢 ⑥提出化学元素的概念 ⑦人工合成牛胰岛素 ⑧火药
A. ①②③④ B. ②④⑦⑧ C. ①⑤⑦⑧ D. ③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气的制取及其性质的微型实验: ①用滤纸剪成四个适当大小的长方形,然后将这些滤纸都用凡士林粘在集气瓶内部。
②将饱和NaI、NaBr、Na2S、品红溶液(1~2滴)滴在如图所示的滤纸上。
③向集气瓶内加1.5 g KClO3 , 用滴管吸取约2 mL浓盐酸,然后将滴管装在双孔塞上,最后把该双孔塞塞在集气瓶上,如图所示。
④用滴管向漏斗中加NaOH溶液,注意所加NaOH溶液应以刚好装满漏斗下端的弯管处为宜(NaOH溶液在此起液封作用同时又有减压功能)
⑤挤压胶头滴管向集气瓶中加浓盐酸。
⑥整个现象看完后,用滴管向漏斗中加NaOH溶液吸收尾气。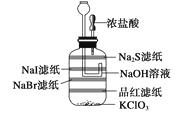
(1)该实验的主要现象: ;
(2)该实验的化学方程式:。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com