
| A. | NaCl溶液 | B. | NaOH溶液 | C. | H2SO4溶液 | D. | CuSO4溶液 |
分析 用石墨作电极,电解下列物质的溶液,通电一段时间后溶液的pH变大,说明该电解质溶液中氢离子浓度减小,则溶液中的电解质不能是含氧酸、含氧酸盐等,结合电解原理来回答.
解答 解:A、电解氯化钠得到的是氢氧化钠溶液,所以碱性增强,pH变大,故A正确;
B、电解氢氧化钠相当于电解水,所以溶液的碱性增加,pH变大,故B正确;
C、电解硫酸相当于电解水,所以溶液的碱性减弱,酸性增加,pH变小,故C错误;
D、电解硫酸铜,得到的是硫酸溶液,所以pH降低,故D错误.
故选AB.
点评 本题考查了电解原理,明确离子放电顺序是解本题关键,根据各个电极上放电的离子结合溶液中氢离子或氢氧根离子浓度变化来分析解答,题目难度不大.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
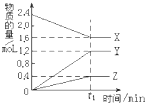 I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示: 3Y+Z.
3Y+Z.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A可被催化氧化为醛 | |
| C. | 维生素A是一种易溶于水的醇 | |
| D. | 1mol维生素A在催化剂作用下最多可与7mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
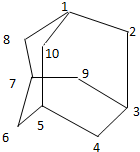 石油中溶有一种碳氢化合物-金刚烷.金刚烷 是一种环状烃,它的结构高度对称.下图表示金刚烷,图中数字是碳原子编号.碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子.
石油中溶有一种碳氢化合物-金刚烷.金刚烷 是一种环状烃,它的结构高度对称.下图表示金刚烷,图中数字是碳原子编号.碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com