

| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届浙江省温州市十校联合体高三上学期期中联考化学试卷(解析版) 题型:填空题
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
|
物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
溶度积 |
2.8×10–9 |
6.8×10–6 |
5.5×10–6 |
1.8×10–11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为 (填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是 ;如果不能直接投入,应将贝壳作何处理,试写出化学方程式 。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为 (填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他 (填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是 (用离子方程式表示)。
(3)已知海水中镁离子浓度为1.8×10–3mol·L–1,则要使镁离子产生沉淀,溶液的PH最低应为 。
查看答案和解析>>
科目:高中化学 来源:2015届北京市东城区高一下学期期末考试化学试卷(解析版) 题型:实验题
从海水提取镁和溴的流程如下,请回答相关问题。
(1)从海水中提取镁的流程如下图所示(框图中是主要产物):
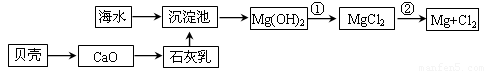
i.海水进入沉淀池前,对海水进行处理有以下两种方案:
方案一:将晒盐后的卤水通入沉淀池;
方案二:将加热蒸发浓缩后的海水通入沉淀池。
你认为方案________更合理,理由是_________________________________________。
ii.反应①的离子方程是________________________________________________。
反应②的化学方程式是_______________________________________________。
(2)从海水中提取溴的流程如下图所示(框图中是主要产物):


i.过程①中,加入的试剂是___________。
ii.过程②中,向混合液中吹入热空气,将溴吹出,用纯碱吸收,吹入热空气的目的是______________________________________________________________________。
iii.过程③中反应的化学方程式是____________________________________________。
iv.若最终得到的溴单质中仍然混有少量的Cl2,则除去该杂质的方法是__________________________________________________(结合离子方程式回答)。
查看答案和解析>>
科目:高中化学 来源:2014届福建省、二中高二上学期期末联考化学试卷(解析版) 题型:填空题
目前世界各国获得镁的主要来源从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:?
|
物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
溶度积 |
2.8×10-9 |
6.8×10-6 |
5.5×10-6 |
1.8×10-11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为 (填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是 。如果不能直接投入,应将贝壳作何处理,试写出化学方程式: 。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为 。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ="=2" Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于 (选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为 。
③该氯化钙样品中钙元素的质量百分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com