
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列有关说法中,正确的是
A.N5+ 离子中含有36个电子 B.H2与H3属于同素异形体
C.C60720 D.O2与O4属于同位素
科目:高中化学 来源: 题型:
把aL含硫酸铵和硝酸铵的混合液分 成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中N03—的物质的量浓度是(单位:mol·L—1)………………………………………………………( )
成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中N03—的物质的量浓度是(单位:mol·L—1)………………………………………………………( )
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中导电性最强的是
A.5L 0.1mol / L NH3·H2O B.5L 0.2mol / L 盐酸
C.0.1L 0.1mol / L 醋酸溶液 D.0.1L 0.1mol / L NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,
下列结论正确的是
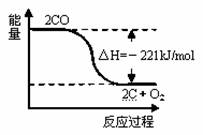
A.碳的燃烧热大于110.5 kJ/mol
B.右图可表示①的反应过程和能量关系
C.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量
查看答案和解析>>
科目:高中化学 来源: 题型:
用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1) 配制待测液:用已称好的5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液。除烧杯和玻棒外,还需要用到的主要仪器有__________,__________;
(2) 滴定过程:
①盛装0.10 mol/L的盐酸标准液应该使用_______滴定管;
②滴定时双眼应注意观察___________________________________;
(3) 误差讨论:(选填“偏高”、“偏低”或“无影响” )
① 用蒸馏水冲洗锥形瓶,测定结果__________;
② 在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果__________;
③ 读数时,滴定前仰视,滴定后俯视,测定结果____________;
④ 装标准液之前,没有用标准液润洗滴定管,测定结果____________;
(4) 有关数据记录如下:
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
计算纯度:烧碱样品的纯度是____________(取两次实验所耗盐酸的平均值进行计算,不写计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
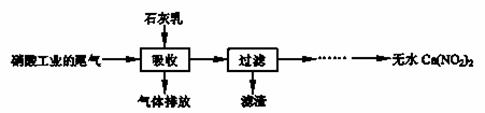
请回答下列问题:
(1)一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)  N2O3(g),其平衡常数表达式为K= 。
N2O3(g),其平衡常数表达式为K= 。
(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底部进入,石灰乳从吸收塔顶部喷淋),其目的是 ;滤渣可循环利用,滤渣的主要成分是 (填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1︰1。若n(NO) :n(NO2)>1︰1,则会导致 ;若n(NO) :n(NO2)<1︰1,则会导致 。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关晶体的说法中,正确的是
A.凡是具有规则外形的固体都是晶体
B.玛瑙属于玻璃体有固定熔点
C.固态氧(O2)和固态硫(S8)都是分子晶体
D.氯化钠和氯化铯都是离子晶体,晶体结构相同
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:卤代烃与活泼金属发生下列反应:

 R—X +2Na + X—R' R—R'+ 2NaX,根据下列各物质的转化关系回答:
R—X +2Na + X—R' R—R'+ 2NaX,根据下列各物质的转化关系回答:
C2H2 B C(2,3—二甲基丁烷)
(1)C2H2→B的反应类型是 ;C的结构简式是 ;
用系统命名法命名B: 。
(2)写化学方程式:B→C: 。
Ⅱ、(7分)(1)氯化铝常温下为固体,熔点190℃(253kPa),易升华。实验室测得氯化铝蒸气的密度为11.92g·L—1(已折算成标准状况),据此判断氯化铝晶体为 晶体,其分子式为 。
(2)氧化镁晶体的晶胞结构与NaCl晶体的晶胞结构相同。则氧化镁晶体中阴离子的配位数为` 个;氧化镁晶体的熔点比NaCl高的原因是
。
(3)金属铁的晶体在不同温度下有右图所示的两种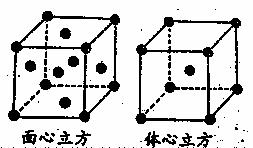
堆积方式,面心立方晶胞和体心立方晶胞中的Fe原
子的配位数之比为 ;两种堆积方式
中密度较大的是 立方堆积。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.铜与稀硝酸的反应:Cu+4H++2NO3-= Cu2++2NO2↑+2H2O
B.氯气与水反应:Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
C.铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
D.铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com