
【题目】根据要求写出下列的方程式。
(1)过氧化钠与水反应的化学方程式:________;
(2)硫酸铝溶液与氨水反应的离子方程式:________;
(3)铁单质与水蒸气反应的化学方程式:________;
(4)二氧化硅与氢氟酸反应的化学方程式:________。
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g)+3Y(g)2Z(g),有关下列图象的说法正确的是( )
A.依据图a可判断正反应为吸热反应
B.在图b中,虚线可表示压强增大
C.若正反应的△H<0,图c可表示升高温度使平衡向逆反应方向移动
D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应:
①SO2+H2O=H2SO3 ②C+H2O=H2+CO
③2Al+6H+=2Al3++3H2↑ ④2Mg+CO2![]() 2MgO+C
2MgO+C
⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥Ca2C2+2H20=Ca(OH)2+C2H2↑
(1)上述反应中不属于氧化还原反应的有_________(填各反应的序号,下同);反应物中H2O被还原的是_______;还原产物为单质的是_______。
(2)上述各反应所涉及到的物质中,属于弱电解质的是______(填化学式)。
(3)用单线桥表示反应④中电子转移的方向和数目___________________。
(4)高铁酸钾(K2FeO4)溶液呈紫红色,向其中加入过量亚硝酸钠,溶液紫红色逐渐褪去,出现红褐色沉淀,溶液的pH逐渐增大。请写出该反应的离子方程式__________________。
(5)下列两组混合物,括号内为杂质,填写除去杂质所需电解质溶液(限定只能用含有钠元素的试剂,假设用量可控),并写出反应的离子方程式。
①Fe2O3(SiO2) 试剂________,________________________________________。
②Na2CO3(NaAlO2) 试剂________,________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 澄清石灰水与过量碳酸氢钠溶液反应:HCO3-+ Ca2+ + OH-![]() CaCO3↓+H2O
CaCO3↓+H2O
B. 工业上氯气和石灰乳反应制漂白粉:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
C. 向硫酸氢钠溶液中滴加氢氧化钡溶液至SO42-沉淀完全:Ba2++2OH-+2H++SO42-![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 硫酸氢钠溶液与小苏打溶液的反应:H++HCO3-![]() H2O+CO2↑
H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于液氯和氯水的叙述正确的是
A.二者为同一种物质B.氯水具有酸性,液氯无酸性
C.久置氯水比新制氯水的漂白性强D.常温下,氯水和液氯均可用钢瓶存放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,铁是使用最广泛的金属之一,已知在高温下,Fe与水蒸气可发生反应.应用如图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 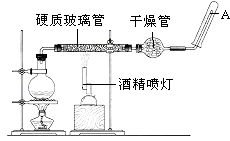
请回答下列的问题.
(1)铁在周期表中的位置是 .
(2)请写出该反应的化学方程式: .
(3)曾利用铝和铁的氧化物反应原理来焊接钢轨,该反应的化学方程式为 .
(4)现有铁和铂组成的合金共a mol,其中Pt的物质的量分数为x,研成粉末状后全部投入含b mol HNO3的稀溶液中,使其充分反应,且HNO3的还原产物只有NO.试回答下列问题: ①随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有四种情况,请用粒子符号填写下表空白:
① | ② | ③ | ④ | |
溶液中的金属离子 | Fe2+ | |||
残留固体成分 | Fe、Pt | Pt | Pt |
②当x=0.5,且溶液中Fe3+与Fe2+和物质的量相等,在标准状况下共产生112mL NO.则a= , b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
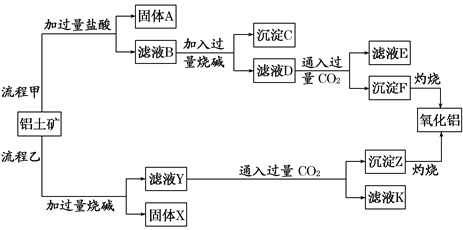
(1)写出流程甲加入盐酸后生成Al3+的离子方程式:___________________________。
(2)写出流程乙加入烧碱后生成SiO![]() 的离子方程式:___________________________。
的离子方程式:___________________________。
(3)为了验证滤液B中含Fe3+,可取少量滤液并加入___________(填试剂名称)。
(4)滤液E 、K中溶质的主要成分是_____(填化学式),写出该溶液的一种用途:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com