
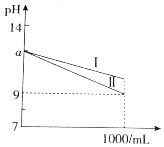
| A. | 曲线Ⅰ表示NaOH溶液中pH的变化 | |
| B. | 开始时两溶液中水的电离程度相同 | |
| C. | 由图象可知,开始时c(NaOH)=0.01mol•L-1 | |
| D. | 在稀释过程中氨水溶液中的$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
分析 A.在室温下取pH=a的NH3•H2O、NaOH溶液各1mL,分别加水稀释到1000mL,一水合氨溶液中存在电离平衡,稀释促进电离,一水合氨又电离出氢氧根离子,PH减小的小;
B.pH=a的NH3•H2O、NaOH溶液各1mL,氢氧根离子浓度相同对水的抑制沉淀相同;
C.氢氧化钠为强碱,图象中氢氧化钠 稀释1000倍,溶液PH为9,原溶液PH=12,结合离子积常数计算氢氧根离子浓度;
D.加水稀释促进电离,促进电离溶液中氢氧根离子浓度减小,$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$×$\frac{c(O{H}^{-})}{c(O{H}^{-})}$,电离平衡常数不变.
解答 解:A.在室温下取pH=a的NH3•H2O、NaOH溶液各1mL,分别加水稀释到1000mL,一水合氨溶液中存在电离平衡,NH3•H2O?NH4++OH-,稀释促进电离,一水合氨又电离出氢氧根离子,PH减小的小,所以曲线Ⅰ表示氨水溶液中pH的变化,曲线Ⅱ表示NaOH溶液中pH的变化,故A错误;
B.pH=a的NH3•H2O、NaOH溶液各1mL,氢氧根离子浓度相同对水的抑制沉淀相同,开始时两溶液中水的电离程度相同,故B正确;
C..氢氧化钠为强碱,图象中氢氧化钠 稀释1000倍,溶液PH为9,原来溶液PH=12,氢氧化钠溶液浓度等于氢氧根离子浓度=$\frac{1{0}^{-14}}{1{0}^{-12}}$=0.01mol/L,故C正确;
D.加水稀释促进电离,促进电离溶液中氢氧根离子浓度减小,电离平衡常数不变,$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$×$\frac{c(O{H}^{-})}{c(O{H}^{-})}$=$\frac{Kb}{c(O{H}^{-})}$,比值增大,故D正确;
故选A.
点评 本题考查了弱电解质电离平衡、平衡常数影响因素、图象分析、溶液稀释后溶液PH变化等知识,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 75 mL 1.5 mol•L-1的MgCl2溶液 | B. | 75 mL 4 mol•L-1的NH4Cl溶液 | ||
| C. | 150 mL 2 mol•L-1的KCl溶液 | D. | 150 mL 1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液、胶体和悬浊液三种分散系的本质区别是分散质微粒直径的大小 | |
| B. | 甲醇和氧气以及KOH溶液构成的新型燃料电池中,其正极上发生的反应为:CH3OH-6e-+8OH-=CO32-+6H2O | |
| C. | 在铁上镀铜时,金属铜作阴极 | |
| D. | 电解法精炼铜时,电解质溶液中铜离子浓度一定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0×l0-15 | B. | 1.0×10-14 | C. | 1.0×10-13 | D. | l.0×l0-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是一种重要的化工原料,广泛应用于自来水的消毒和农药的生产等方面 | |
| B. | 钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂 | |
| C. | 用二氧化硅制造的光导纤维具有很强的导电能力,可用于制作光缆 | |
| D. | 化肥的生产、金属矿石的处理、金属材料的表面清洗等都可能用到硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14Cl与16O具有相同的中子数 | |
| B. | ${\;}_{50}^{119}Sn$与${\;}_{82}^{207}Pb$具有相同最外层电子数 | |
| C. | NH4+与OH-具有相同的质子数和电子数 | |
| D. | O22-和S2-具有相同的质子数和电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com