
| A、H2O2溶液有氧化性,可用于杀菌消毒 |
| B、氯化镁是一种电解质,可用于电解法制镁 |
| C、液氨汽化时要吸收大量的热,可用作制冷剂 |
| D、Na2SO4能使蛋白质发生变性,可用于提纯蛋白质 |


科目:高中化学 来源: 题型:
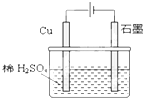
| A、电解过程中,铜电极上没有H2产生 | ||||
B、电解初期,主反应方程式为:Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,H+的浓度不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 |
| B、常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| C、硝酸与金属反应时,主要是+5价的氮得电子 |
| D、浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
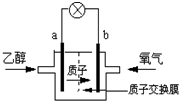 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )| A、b极为电池的负极 |
| B、设每个电子所带电量为q库仑,则1mol乙醇被氧化产生12NAq库仑的电量 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:O2+4e-+2H2O=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子晶体中一定不含离子键,但一定存在共价键 |
| B、熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C、NCl3分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数比是1:2,且熔化时破坏的是离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:N3->Na+>H+ |
| B、与水反应都是氧化还原反应 |
| C、与盐酸反应都只生成一种盐 |
| D、两种化合物中的阴阳离子均具有相同的电子层结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com