
[15·Ц]»ҜәПОпXКЗТ»ЦЦ»·ҫіјӨЛШЈ¬ҙжФЪИзПВЧӘ»Ҝ№ШПөЈә
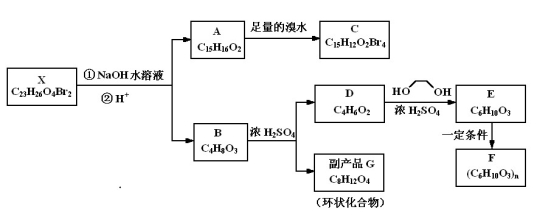
»ҜәПОпAДЬУлFeCl3ИЬТә·ўЙъПФЙ«·ҙУҰЈ¬·ЦЧУЦРә¬УРБҪёц»ҜС§»·ҫіНкИ«ПаН¬өДјЧ»щЈ¬ЖдұҪ»·ЙПөДТ»Пх»щИЎҙъОпЦ»УРБҪЦЦЎЈ1H-NMRЖЧПФКҫ»ҜәПОпGөДЛщУРЗвФӯЧУ»ҜС§»·ҫіПаН¬ЎЈFКЗТ»ЦЦҝЙУГУЪЦЖұёТюРОСЫҫөөДёЯҫЫОпЎЈ
ёщҫЭТФЙПРЕПў»ШҙрПВБРОКМвЎЈ
ЈЁ1Ј©ПВБРРрКцХэИ·өДКЗ_________ЎЈ
AЈ®»ҜәПОпA·ЦЧУЦРә¬УРБӘұҪҪб№№өҘФӘ
BЈ®»ҜәПОпAҝЙТФәНNaHCO3ИЬТә·ҙУҰЈ¬·ЕіцCO2ЖшМе
CЈ®XУлNaOHИЬТә·ҙУҰЈ¬АнВЫЙП1 mol XЧо¶аПыәД6 mol NaOH
DЈ®»ҜәПОпDДЬУлBr2·ўЙъјУіЙ·ҙУҰ
ЈЁ2Ј©»ҜәПОпCөДҪб№№јтКҪКЗ_________________Ј¬AЎъCөД·ҙУҰАаРНКЗ________ЎЈ
ЈЁ3Ј©РҙіцН¬КұВъЧгПВБРМхјюөДDөДЛщУРН¬·ЦТм№№МеөДҪб№№јтКҪЈЁІ»ҝјВЗБўМеТм№№_________ЎЈ
aЈ®КфУЪхҘАаbЈ®ДЬ·ўЙъТшҫө·ҙУҰ
ЈЁ4Ј©РҙіцBЎъC·ҙУҰөД»ҜС§·ҪіМКҪ_______________________________________________ЎЈ
ЈЁ5Ј©РҙіцEЎъF·ҙУҰөД»ҜС§·ҪіМКҪ_______________________________________________ЎЈ
(15·Ц)
(1)cd
(2)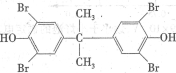 ЎЎЎЎЎЎЎЎИЎҙъ·ҙУҰ
ЎЎЎЎЎЎЎЎИЎҙъ·ҙУҰ
(3)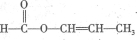 ЎЎЎЎЎЎ
ЎЎЎЎЎЎ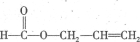 ЎЎЎЎЎЎ
ЎЎЎЎЎЎ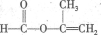 ЎЎ
ЎЎ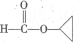
(4)
(5)
ЎҫҪвОцЎҝұИҪПЈБУлЈГҝЙ·ўПЦЈГұИЈБ¶аБЛЈҙёцBrЈ¬ЙЩБЛЈҙёцЈИЈ¬ЛөГч·ўЙъБЛИЎҙъ·ҙУҰЈ¬ҝЙіхІҪНЖ¶ПФЪЈБөДҪб№№ЦРә¬УРЈІёц·УөДҪб№№өҘФӘЈ¬ЗТЖд¶ФО»ҝЙДЬКөХјҫЭЈ»ФЩ·ЦОцЈБЎўЈВУлЈШЦ®јдөД№ШПөЈ¬ҝЙНЖІвЈШЦРҫЯУРхҘөДҪб№№Ј¬ЈБЦРөДЈІёцфЗ»щУлЈВЦРөДфИ»щНСЛ®іЙхҘөДҪб№№Ј¬¶шЈШ·ЦЧУөДBrФӯЧУЛ®ҪвөГөҪөДфЗ»щ»бФЪЈВ·ЦЧУЦРЈ¬јҙЈВЦРјИә¬УРфИ»щЈ¬»№ә¬УРфЗ»щЈ¬ЛщТФЈВФЪЕЁБтЛбҙжФЪөДМхјюПВНЁ№эПыИҘНСЛ®ҝЙөГЦчТӘІъОпЈДЈ¬НЁ№э·ЦЧУјдНСЛ®хҘ»ҜөГёұІъЖ·ЈЗЈ¬ЈДЦРә¬УРЛ«јьЈ¬ЈЗЦРә¬УР»·хҘҪб№№Ј»ЈДУлHOCH2CH2OH·ўЙъхҘ»Ҝ·ҙУҰЈ¬өГөҪә¬УРЛ«јьҪб№№өДхҘEЈ¬хҘEФтДЬНЁ№эјУҫЫ·ҙУҰөГөҪёЯ·ЦЧУ»ҜәПОпFЎЈҫӯТФЙП·ЦОцҝЙөГAЈӯGөДёчОпЦК·ЦұрОӘЈ¬AКЗ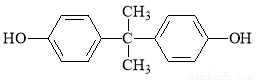 Ј¬BКЗ
Ј¬BКЗ Ј¬CКЗ
Ј¬CКЗ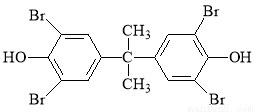 Ј¬DКЗ
Ј¬DКЗ Ј¬EКЗ
Ј¬EКЗ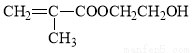 Ј¬FКЗ
Ј¬FКЗ Ј¬GКЗ
Ј¬GКЗ ЎЈЈЁ1Ј©·ЦОцAЎўDЎўXҪб№№ҝЙЦӘЈ¬AІ»КфУЪМюј°AЦРЦ»УР·УҪб№№Ј¬aЎўbПоҙнОуЈ»XЦРУР¶юёцхҘҪб№№Ј¬ЗТЛ®ҪвәуөГөҪ·УАаОпЦКЈ¬ЛщТФҝЙТФПыәД4molNaOHЈ¬ФЩјУЙП2ёцдеФӯЧУЛ®ҪвТІҝЙПыәД2molNaOHЈ¬cПоХэИ·Ј»DЦРә¬УРЛ«јьЈ¬ҝЙУлде·ўЙъјУіЙ·ҙУҰЈ¬dПоХэИ·Ј»ЈЁ2Ј©AЧӘұдОӘCөД·ҙУҰКЗИЎҙъ·ҙУҰЈ»ЈЁ3Ј©УРхҘҪб№№ЗТҫЯУРИ©»щөДОпЦКУҰёГКЗјЧЛбхҘЈ¬DөДН¬·ЦТм№№МеУРЈә
ЎЈЈЁ1Ј©·ЦОцAЎўDЎўXҪб№№ҝЙЦӘЈ¬AІ»КфУЪМюј°AЦРЦ»УР·УҪб№№Ј¬aЎўbПоҙнОуЈ»XЦРУР¶юёцхҘҪб№№Ј¬ЗТЛ®ҪвәуөГөҪ·УАаОпЦКЈ¬ЛщТФҝЙТФПыәД4molNaOHЈ¬ФЩјУЙП2ёцдеФӯЧУЛ®ҪвТІҝЙПыәД2molNaOHЈ¬cПоХэИ·Ј»DЦРә¬УРЛ«јьЈ¬ҝЙУлде·ўЙъјУіЙ·ҙУҰЈ¬dПоХэИ·Ј»ЈЁ2Ј©AЧӘұдОӘCөД·ҙУҰКЗИЎҙъ·ҙУҰЈ»ЈЁ3Ј©УРхҘҪб№№ЗТҫЯУРИ©»щөДОпЦКУҰёГКЗјЧЛбхҘЈ¬DөДН¬·ЦТм№№МеУРЈә Ј¬
Ј¬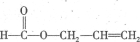 Ј¬
Ј¬ Ј¬
Ј¬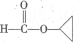 Ј»ЈЁ4Ј©BЎъC·ҙУҰөД»ҜС§·ҪіМКҪОӘ
Ј»ЈЁ4Ј©BЎъC·ҙУҰөД»ҜС§·ҪіМКҪОӘ Ј»ЈЁ5Ј©EЎъF·ҙУҰөД»ҜС§·ҪіМКҪОӘ
Ј»ЈЁ5Ј©EЎъF·ҙУҰөД»ҜС§·ҪіМКҪОӘ ЎЈ
ЎЈ
Ўҫҝјөг¶ЁО»ЎҝұҫМвҝјІйУР»ъНЖ¶ПәННЖАнДЬБҰЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2013-2014ЙПәЈКРұҰЙҪЗшёЯ¶юДкј¶»ҜѧѧҝЖЦКБҝјаІв»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
І»ДЬУГАлЧУ·ҪіМКҪCO32Јӯ+2H+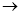 CO2Ўь+H2OұнКҫөДКЗ
CO2Ўь+H2OұнКҫөДКЗ
A. Na2CO3+2HCl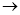 2NaCl +CO2Ўь+H2O B. NaHCO3+HCl
2NaCl +CO2Ўь+H2O B. NaHCO3+HCl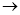 NaCl +CO2Ўь+H2O
NaCl +CO2Ўь+H2O
C. K2CO3+H2SO4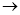 K2SO4 +CO2Ўь+H2O D. K2CO3+2HNO3
K2SO4 +CO2Ўь+H2O D. K2CO3+2HNO3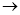 2KNO3 +CO2Ўь+H2O
2KNO3 +CO2Ўь+H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁЦШЗмҫнҪвОц°жЈ© МвРНЈәСЎФсМв
ЈЁ6·ЦЈ©ЈЁ2012?ЦШЗмЈ©лВЈЁH2N©ҒNH2Ј©КЗТ»ЦЦёЯДЬИјБПЈ¬УР№Ш»ҜС§·ҙУҰөДДЬБҝұд»ҜИзНјЛщКҫЈ¬ТСЦӘ¶ПБС1mol»ҜС§јьЛщРиөДДЬБҝЈЁkJЈ©ЈәNЎФNОӘ942ЎўO=OОӘ500ЎўN©ҒNОӘ154Ј¬Фт¶ПБС1molN©ҒHјьЛщРиөДДЬБҝЈЁkJЈ©КЗЈЁ Ј©
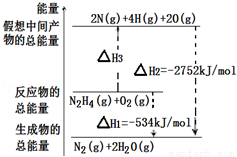
A.194 B.391 C.516 D.658
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁәЈДПҫнҪвОц°жЈ© МвРНЈәСЎФсМв
ДЬХэИ·ұнКҫПВБР·ҙУҰөДАлЧУ·ҪіМКҪОӘ
AЈ®МјЛбЗвДЖИЬТәЦРөОИлЗвСх»ҜёЖИЬТәЈәHCO3-+OHЁC= CO32-+ H2O
BЈ®¶юСх»ҜБтНЁИлҙОВИЛбДЖИЬТәЈәSO2 + ClO- + 2OHЁC= SO42-+Cl-+ H2O
CЈ®Бт»ҜұөјУИлПЎБтЛбЈәBaS+ 2H+ = H2SЎь+ Ba2+
DЈ®РВЦЖөДСх»ҜВБҝЙИЬУЪЗвСх»ҜДЖИЬТәЈәAl2O3+2OHЁC=2AlO2ЁC+H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁәЈДПҫнҪвОц°жЈ© МвРНЈәСЎФсМв
·ЦЧУКҪОӘC10H14өДөҘИЎҙъ·јМюЈ¬ЖдҝЙДЬөДҪб№№УР
AЈ®2ЦЦ BЈ®3ЦЦ CЈ®4ЦЦ DЈ®5ЦЦ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁХгҪӯҫнҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРЛө·ЁХэИ·өДКЗ
AЈ®іЈОВПВЈ¬Ҫ«pHЈҪ3өДҙЧЛбИЬТәПЎКНөҪФӯМе»эөД10ұ¶әуЈ¬ИЬТәөДpHЈҪ4
BЈ®ОӘИ·¶ЁДіЛбH2AКЗЗҝЛб»№КЗИхЛбЈ¬ҝЙІвNaHAИЬТәөДpHЎЈИфpHЈҫ7Ј¬ФтH2AКЗИхЛбЈ»ИфpHЈј7Ј¬ФтH2AКЗЗҝЛб
CЈ®УГ0.2000 mol/L NaOHұкЧјИЬТәөО¶ЁHClУлCH3COOHөД»мәПИЬТәЈЁ»мәПТәЦРБҪЦЦЛбөДЕЁ¶ИҫщФјОӘ0.1 mol/LЈ©,ЦБЦРРФКұЈ¬ИЬТәЦРөДЛбОҙұ»НкИ«ЦРәН
DЈ®ПаН¬ОВ¶ИПВЈ¬Ҫ«ЧгБҝВИ»ҜТш№ММе·Цұр·ЕИлПаН¬Ме»эөДўЩХфБуЛ®ЎўўЪ0.1mol/LСОЛбЎўўЫ0.1 mol/LВИ»ҜГҫИЬТәЎўўЬ0.1mol/LПхЛбТшИЬТәЦРЈ¬AgЈ«ЕЁ¶ИЈәўЩЈҫўЬЈҪўЪЈҫўЫ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁРВҝОұкҪвОц°жЈ© МвРНЈәјтҙрМв
ЎҫСЎРЮ3ОпЦКҪб№№УлРФЦКЎҝЈЁ15·ЦЈ©
VIAЧеөДСхЎўБтЎўОш(Se)ЎўнЪ(Te)өИФӘЛШФЪ»ҜәПОпЦРіЈұнПЦіц¶аЦЦСх»ҜМ¬Ј¬ә¬VIAЧеФӘЛШөД»ҜМЁОпФЪСРҫҝәНЙъІъЦРУРРн¶аЦШТӘУГНҫЎЈЗл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©SөҘЦКөДіЈјыРОКҪОӘS8Ј¬Жд»·ЧҙҪб№№ИзПВНјЛщКҫЈ¬SФӯЧУІЙУГөД№мөАФУ»Ҝ·ҪКҪКЗ Ј»

ЈЁ2Ј©ФӯЧУөДөЪТ»өзАлДЬКЗЦёЖшМ¬өзЦРРФ»щМ¬ФӯЧУК§ИҘТ»ёцөзЧУЧӘ»ҜОӘЖшМ¬»щМ¬ХэАл
ЧУЛщРиТӘөДЧоөНДЬБҝЈ¬OЎўSЎўSeФӯЧУөДөЪТ»өзАлДЬУЙҙуөҪРЎөДЛіРтОӘ Ј»
ЈЁ3Ј©SeФӯЧУРтКэОӘ Ј¬ЖдәЛНвMІгөзЧУөДЕЕІјКҪОӘ Ј»
ЈЁ4Ј©H2SeөДЛбРФұИH2S ЈЁМоЎ°ЗҝЎұ»тЎ°ИхЎұЈ©ЎЈЖшМ¬SeO3·ЦЧУөДБўМе№№РН
ОӘ Ј¬SO32-АлЧУөДБўМе№№РНОӘ Ј»
ЈЁ5Ј©H2SeO3өДK1әНK2·ЦұрОӘ2.7x l0-3әН2.5x l0-8Ј¬H2SeO4өЪТ»ІҪјёәхНкИ«өзАлЈ¬
K2ОӘ1.2X10-2Ј¬ЗлёщҫЭҪб№№УлРФЦКөД№ШПөҪвКНЈә
ўЩH2SeO3әНH2SeO4өЪТ»ІҪөзАліМ¶ИҙуУЪөЪ¶юІҪөзАлөДФӯТтЈә
Ј»
ўЪ H2SeO4ұИ H2SeO3ЛбРФЗҝөДФӯТтЈә
ЈЁ6Ј©ZnSФЪУ«№вМеЎў№вөјМеІДБПЎўНҝБПЎўСХБПөИРРТөЦРУҰУГ№г·әЎЈБў·ҪZnSҫ§МеҪб№№ИзПВНјЛщКҫЈ¬Ждҫ§°ыұЯіӨОӘ540.0 pmЈ®ГЬ¶ИОӘ ЈЁБРКҪІўјЖЛгЈ©Ј¬aО»ЦГS2-АлЧУУлbО»ЦГZn2+АлЧУЦ®јдөДҫаАлОӘ pmЈЁБРКҫұнКҫЈ©
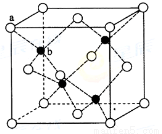
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012ДкЖХНЁёЯөИѧУХРЙъИ«№ъНіТ»ҝјКФ»ҜС§ЈЁ№г¶«ҫнҪвОц°жЈ© МвРНЈәСЎФсМв
ЈЁ6·ЦЈ©ЈЁ2012?№г¶«Ј©ИзНјКЗІҝ·Ц¶МЦЬЖЪФӘЛШ»ҜәПјЫУлФӯЧУРтКэөД№ШПөНјЈ¬ПВБРЛө·ЁХэИ·өДКЗЈЁЎЎЎЎЈ©
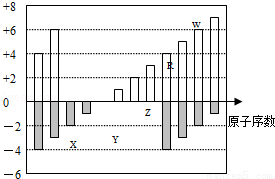
A.ФӯЧУ°лҫ¶ЈәZЈҫYЈҫX
B.ЖшМ¬Зв»ҜОпөДОИ¶ЁРФЈәRЈҫW
C.WX3әНЛ®·ҙУҰРОіЙөД»ҜәПОпКЗАлЧУ»ҜәПОп
D.YәНZБҪХЯЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпДЬПа»Ҙ·ҙУҰ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2012-2014ЛДҙЁКЎТЛІэКРҙәјҫЖЪЦРҝјКФёЯТ»»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ЖыіөөДЖф¶ҜөзФҙіЈУГЗҰРоөзіШЎЈЖдҪб№№ИзПВНјЛщКҫЈ¬·ЕөзКұөДөзіШ·ҙУҰИзПВЈәPbO2Ј«PbЈ«2H2SO4=2PbSO4Ј«2H2OёщҫЭҙЛ·ҙУҰЕР¶ППВБРРрКцЦРХэИ·өДКЗ
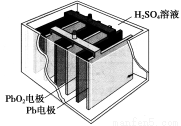
AЈ®PbO2КЗөзіШөДёәј«
BЈ®·ЕөзКұЈ¬ИЬТәЦРөДH+ПтХэј«ЗшТЖ¶ҜЈ¬Хэј«ЗшУтөДИЬТәөДЛбРФФцЗҝ
CЈ®·ЕөзКұЈ¬өзЧУУЙPbөзј«НЁ№эөјПЯБчПтPbO2
DЈ®Хэј«өДөзј«·ҙУҰКҪОӘPb-2eЈӯ=Pb2+
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com