
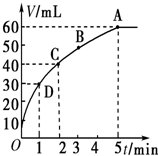
 l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示.
l mol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g?L-1),在标准状况下,放出气体的体积y和时间t的关系曲线如图所示.
| ||
| V |
| Vm |
| n |
| V |
| ||
| 0.06L |
| 22.4L/mol |
| 0.06 |
| 22.4 |
| ||
| 0.06 |
| 22.4 |
| 0.06 |
| 11.2 |
| ||
| 0.05L |


科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下:
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
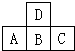 如图中A、B、C、D是短周期中同周期或同主族的相邻元素.
如图中A、B、C、D是短周期中同周期或同主族的相邻元素.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| B、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=c(H+)+c(CH3COOH) |
| D、pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com