
【题目】下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是
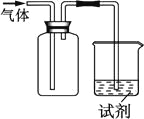
选项 | 气体 | 试剂 | 现象 | 结论 |
A | NO | 紫色石蕊试液 | 溶液变红 | NO与水反应生成硝酸 |
B | Cl2 | KI淀粉溶液 | 溶液变蓝 | Cl2有氧化性 |
C | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2有漂白性 |
D | NH3 | 酚酞试剂 | 溶液变红 | NH3有碱性 |
A.AB.BC.CD.D
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.25℃时,测得0.1mol/L的一元碱MOH溶液pH=11,则MOH一定为弱碱
B.25℃时,将pH=1的H2SO4溶液加水稀释10倍,所得溶液的c(SO42-)为0.005mol/L
C.25℃时,将![]() 的一元碱MOH溶液加水稀释至pH=10,所得溶液c(OH-)=10-4mol/L
的一元碱MOH溶液加水稀释至pH=10,所得溶液c(OH-)=10-4mol/L
D.25℃时,pH=12的一元碱MOH溶液与pH=2的盐酸等体积混合,所得溶液pH≤7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
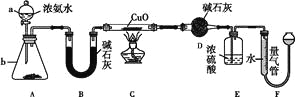
(1)仪器a的名称为____,仪器b中可选择的试剂为____。
(2)实验室中,利用装置A,还可制取的无色气体是____(填字母)。
A.Cl2 | B.O2 | C.CO2 | D.NO2 |
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式:_______________________。
(4)E装置中浓硫酸的作用是_____________________________________。
(5)读取气体体积前,应对装置F进行的操作:____________________________。
(6)实验完毕,若测得干燥管D增重m g,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为____(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到20mL1mol/L的盐酸中,待合金完全溶解后,往溶液里加入1mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法不正确的是( )

A. 镁、铝形成合金后硬度增强,熔点降低B. ab段可以计算出合金中Mg的含量
C. c值越大,合金中Al的含量越高D. 加入NaOH溶液后,只发生了4个离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的质量分数,设计如下两种实验方案。
(1)已知AlN与NaOH反应得到一种盐和一种碱性气体,化学反应方程式是____
(方案1)取一定量的样品,用图1装置测定样品中AlN的质量分数(夹持仪器已略去)。
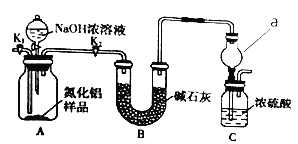

(2)图1中仪器a的名称是___
(3)完成以下实验步骤:组装好实验装置,首先检查装置气密性,再加入实验药品。关闭K1,打开K2和分液漏斗活塞,加入NaOH浓溶液至不再产生气体,打开K1,通入氮气一段时间,测定C装置在反应前后的质量变化。通入氮气的目的是____
(4)由于装置存在缺陷,导致测定结果偏高,请提出改进意见____
(方案2)用图2装置测定mg样品中AlN的质量分数(部分夹持装置己略去)。
(5)为测定生成气体的体积,量气装置中的X液体可以是___(填字母序号)。
a.CCl4 b.H2O c.饱和NH4Cl溶液 d.苯
(6)若mg样品完全反应,测得生成气体的体积为VmL(标准状况),则AlN的质量分数为___。若将b处胶管用弹簧夹夹住,其他操作均不变,则最终测定的结果___(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如下实验探究某矿石(仅含四种短周期元素)的组成和性质,已知矿石含有一定的结晶水:
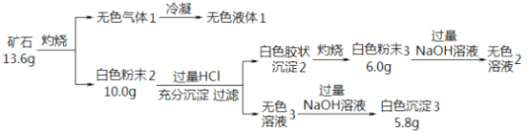
(1)矿石的组成元素是 H、O 和_____、 ______(填元素符号),化学式为_____________。
(2)白色粉末3 溶于NaOH溶液的离子方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理、装置、操作或结论的描述,错误的是
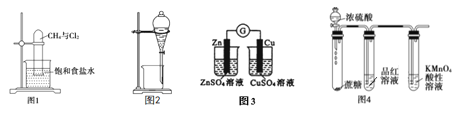
A. 图1所示装置可实现甲烷与氯气在光照条件下的取代反应
B. 图2所示装置可分离CH3COONa溶液和CH3COOC2H5的混合液
C. 图3是原电池装置,有明显的电流
D. 图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的![]() 质量进行计算.某同学设计的实验装置示意图如下:
质量进行计算.某同学设计的实验装置示意图如下:
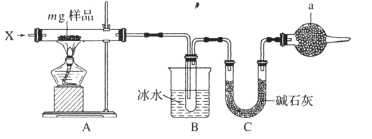
请回答:
(1)A中发生反应的化学方程式是__________________________。
(2)装置B中冰水的作用是_________________________。
(3)该同学设计的实验装置存在缺陷,改进后该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是________________(填字母)。
A.样品分解不完全
B.产生![]() 的速率太快,没有被碱石灰完全吸收
的速率太快,没有被碱石灰完全吸收
C.反应完全后停止加热,通入过量的空气.
(4)若C中的碱石灰改用足量![]() 固体,请设计实验方案检验反应后C中固体的成分___________。
固体,请设计实验方案检验反应后C中固体的成分___________。
(5)检验样品中是否还含有NaHCO3,请选择下列装置设计实验,并完成下表:
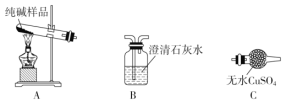
选择的装置(填编号) | 实验现象 | 实验结论 |
①_______________________________ | ②_________________ | 样品中含NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组欲从含有铁的氧化物及少量FeS、SiO2的烧渣中分离出二氧化硅并制备绿矾(FeSO4·7H2O)固体,实验过程如下:

已知:一定条件下固体硫可溶于氢氧化钠溶液。请回答:
(1)步骤①中,试剂X应采用________。
(2)制备绿矾时,向溶液1中加入过量试剂Y,充分反应后,经________操作得到溶液2。
(3)设计简单实验方案验证步骤②得到的SiO2固体中不含S________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com