
 的命名正确的是( )
的命名正确的是( )| A. | 2,3,3-三甲基戊烷 | B. | 2-二甲基-3-乙基丁烷 | ||
| C. | 2,2-二甲基-3-乙基丁烷 | D. | 3,4,4-三甲基戊烷 |
分析 烷烃的命名方法是:
①选主链:找准一“长”一“多”,即碳链最长,支链最多.
从分子中找出最长碳链作为主链.若有几条等长碳链,则应当选择支链最多的作为主链.
②编C号:比较一“近”一“小”,即离支链最近,支链位号之和最小.
从离支链最近的一端开始对主链C原子进行编号.若主链两端离支链的距离一样,则应当选择支链位置号数总和较小的编号方向.
③写名称:基名同,要合并;逗号隔,短线分;先简后繁不要争.
取代基名称相同的要合并写,不同位置之间以“,”隔开,阿拉伯数字与汉字之间以“-”分开;取代基按先简后繁顺序书写.
解答 解:选主链:最长的碳链含有5个C;
编号:从右边编号支链编号之和比从左边编号小,所以从右边编号;
该有机物的名称为:2,3,3-三甲基己戊烷,
故选A.
点评 本题考查了烷烃的命名,难度不大,要求学生熟练掌握烷烃的命名方法,命名中必须满足主链最长,取代基编号之和最小原则.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2NO2+2NaOH═NaNO3+NaNO2+H2O | |
| B. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2 | |
| C. | CaH2+2H2O═Ca(OH)2+2H2↑ | |
| D. | 3CCl4+K2Cr2O7═2CrO2Cl2+3COCl2+2KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | A的转化率变小 | B. | 平衡向逆反应方向移动 | ||
| C. | D的体积分数变大 | D. | a+b>c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
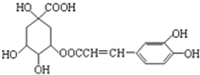 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )| A. | 分子式为C16H13O9 | |
| B. | 与浓溴水既能发生取代反应又能发生加成反应 | |
| C. | 1 mol咖啡鞣酸水解时可消耗8 mol NaOH | |
| D. | 能使酸性KMnO4溶液褪色,说明分子结构中有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加甲基橙试剂显红色的溶液中:Na +、Fe2+、Cl-、NO3- | |
| B. | 由水电离的c(H+)=1.0×10-13mol•L-1的溶液中:K +、Na +、AlO2-、CO3 2- | |
| C. | 常温下,pH=7 溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | KW/c(H+)=0.1 mol•L-1的溶液:Na+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打在生活中可用做发酵粉 | |
| B. | 过氧化钠可用于呼吸面具中氧气的来源 | |
| C. | 可溶性铁盐或铝盐可用于净水 | |
| D. | 二氧化硅可用于制作硅芯片和光电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁达尔效应可以区别溶液和胶体 | |
| B. | NaHCO3溶液中含有少量Na2CO3,可以用澄清石灰水除去 | |
| C. | 金属铝的生产是以Al2O3为原料,在熔融状态下进行电解 | |
| D. | 向品红溶液中通入SO2气体红色褪去,再加热恢复红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
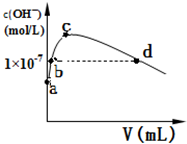 CO2和CH4在一定条件下合成乙酸:CO2+CH4$\stackrel{TiO_{2}/Cu_{2}Al_{2}O_{4}}{→}$CH3COOH.完成下列填空:
CO2和CH4在一定条件下合成乙酸:CO2+CH4$\stackrel{TiO_{2}/Cu_{2}Al_{2}O_{4}}{→}$CH3COOH.完成下列填空: .
. ;其熔沸点比CO2高,原因是二者都为分子晶体,相对分子质量越大,分子间作用力越大.
;其熔沸点比CO2高,原因是二者都为分子晶体,相对分子质量越大,分子间作用力越大. 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
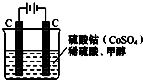 (1)甲醇(CH3OH)是重要的能源物质,研究甲醇具有重要意义.为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-.电池工作时正极反应式为O2+4e-=2O2-.
(1)甲醇(CH3OH)是重要的能源物质,研究甲醇具有重要意义.为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-.电池工作时正极反应式为O2+4e-=2O2-.| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com