
【题目】甲、乙两个化学兴趣小组,分别做乙醇催化氧化并验证产物的实验。甲组实验设计如图1所示,乙组实验设计如图2所示,密闭系统内空气很少。请填写下列空白:
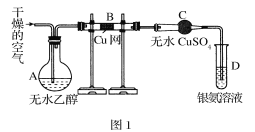

(1)甲组要完成全部实验内容,以下步骤中正确的顺序是 _____ (填序号,步骤可重复)。
①加热 ②检查装置的气密性 ③向A中缓缓鼓入干燥的空气 ④取下D装置
(2)甲、乙两组实验中,给定的A~H中需要加热的是________(填编号)。
(3)反应开始后,C中观察到的现象是________。
(4)写出E中发生反应的化学方程式________。
【答案】②①③④①(或②③①④①) A、B、E、H CuSO4粉末变为蓝色 CH3CH2OH+CuO![]() CH3CHO+H2O+Cu
CH3CHO+H2O+Cu
【解析】
(1)气体制备与性质检验实验的一般步骤:组装仪器、检验装置气密性、气体制取和检验据此排序;
(2)依据反应原理乙醇与氧气在铜做催化剂条件下生成乙醛和水,需要通过加热乙醇液体提供乙醇蒸汽,乙醇的催化氧化需要加热;
(3)白色的无水硫酸铜与水反应生成蓝色的五水硫酸铜;
(4)氧化铜与乙醇加热生成铜、水和乙醛。
(1)完成乙醇催化氧化并验证产物的实验,组装完仪器后应先检查装置气密性,然后制备乙醛,用空气将乙醇蒸汽鼓入B中,在铜做催化剂条件下加热生成乙醛和水,用无水硫酸铜检验水的生成,最后用新制的银氨溶液检验乙醛的生成,所以正确的顺序为:②①③④①(或②③①④①);
故答案为:②①③④①(或②③①④①);
(2)依据反应原理乙醇与氧气在铜做催化剂条件下生成乙醛和水,需要通过加热乙醇液体提供乙醇蒸汽,乙醇的催化氧化需要加热,甲、乙两组实验中,给定的A~H中需要加热的是:A、B、E、H;
故答案为:A、B、E、H;
(3)反应开始后,白色的无水硫酸铜与水反应生成蓝色的五水硫酸铜,所以看到的现象为:CuSO4粉末变为蓝色;
故答案为:CuSO4粉末变为蓝色;
(4)E中发生反应是氧化铜与乙醇加热生成铜、水和乙醛,方程式:CH3CH2OH+CuO![]() CH3CHO+H2O+Cu,故答案为:CH3CH2OH+CuO
CH3CHO+H2O+Cu,故答案为:CH3CH2OH+CuO![]() CH3CHO+H2O+Cu。
CH3CHO+H2O+Cu。


科目:高中化学 来源: 题型:
【题目】现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有如下情况:
(1)X、Y、Z的单质在常温下均为气体
(2)X的单质在Z的单质中燃烧,火焰呈苍白色.产物XZ的水溶液可使石蕊试液变红.
(3)两摩尔X的单质可与一摩尔Y的单质化合生成两摩尔X2Y,X2Y常温下为液体.
(4)Z的单质溶于X2Y中所得溶液具有漂白性.
(5)A的单质可以在Z的单质中燃烧,生成棕红色固体,该固体溶于水呈黄色溶液.
(6)B与Z形成的化合物BZ3溶于水后逐滴滴加NaOH溶液先生成白色沉淀后又逐渐溶解.
(7)C的单质与Y单质反应可能得到两种产物,其中一种为淡黄色固体M.
请完成下列问题:
(1)写出下列物质的化学式:XZ__________,X2Y_________,M_________
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是____________(填化学式)
(3)A的单质与Z的单质反应的化学方程式:________________________________
(4)BZ3与过量的NaOH溶液反应的离子方程式:__________________________
(5)X单质与Z单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,求原混合气体中X单质与Z单质的体积比可能为______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如下图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
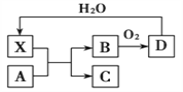
A. X使蔗糖变黑的现象主要体现了X的强氧化性
B. 若A为铁,则足量A与X在室温下即可完全反应
C. 若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到白色沉淀产生
D. 工业上,B转化为D的反应条件为高温、常压、使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠 (Na2S2O3)在生产生活中具有广泛应用。硫化碱法是工业上制取硫代硫酸钠的方法之一。实验室模拟工业生产装置如图所示:
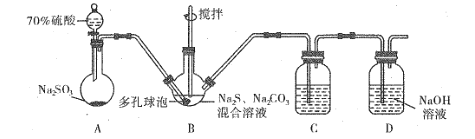
(1)利用如图装置进行实验,为保证硫酸顺利滴下的操作是_______。
(2)装置B中生成的Na2S2O3同时还生成CO2,反应的离子方程式为_______;在该装置中使用多孔球泡的目的是_____。
(3)装置C的作用是检验装置B中SO2的吸收效果,C中可选择的试剂是__(填字母)。
a.H2O2溶液 b.溴水 c.KMnO4溶液 d.BaCl2溶液
(4)Na2S2O3溶液常用于测定废水中Ba2+浓度。
①取废水20.00mL,控制适当的酸度,加入足盐K2Cr2O7溶液,得到 BaCrO4 沉淀,过滤洗涤后用适量稀酸溶解,此时 CrO42-全部转化为Cr2O72-;再加过量 KI溶液,将Cr2O72- 充分反应;然后加入淀粉溶液作指示剂,用0.100 mol/L的Na2S2O3 溶液进行滴定:(I2 +2 S2O32-= S4O62-+ 2I-),滴定终点的现象为__________。平行滴定3次,消耗Na2S2O3 溶液的平均用量为18.00mL。则该废水中Ba2+ 的物质的量浓度为____mol/L,
②在滴定过程中,下列实验操作会造成实验结果偏高的是______(填字母)。
a.滴定管未用Na2S2O3溶液润洗
b.滴定终点时俯视读数
c.锥形瓶用蒸馏水洗涤后未进行干燥处理
d.滴定管尖嘴处滴定前无气泡,滴定终点发现有气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
B.有机物![]() 的消去产物有两种
的消去产物有两种
C.有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH—COOCH3
D.可用溴水鉴别甲苯、苯酚、1-己烯三种无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
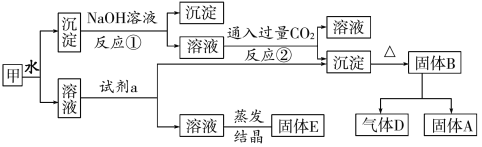
请回答下列问题:
(1)写出A、B、的化学式:A_____________, B_____________。
(2)试剂a最好选用______________。
A、NaOH溶液 B、稀盐酸
C、二氧化碳 D、氨水
(3)写出反应①的离子方程式:____________________。
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛是二十一世纪的“明星金属”,工业制备金属钛是以金红石为原料,发生的反应如下。
反应Ⅰ:aTiO2+bCl2+cC![]() aTiCl4+cCO
aTiCl4+cCO
反应Ⅱ:TiCl4+2Mg ![]() Ti+2MgCl2
Ti+2MgCl2
下列关于反应Ⅰ、Ⅱ的说法中正确的是 ( )
A.反应Ⅰ中TiO2是氧化剂
B.TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂
C.a=b=c=2
D.每生成9.6 g Ti,反应Ⅱ中转移了0.6 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含0.2molAlCl3的溶液中加入了一定量的1mol/L的NaOH溶液后,生成了7.8g的沉淀,则加入的NaOH溶液的体积可能为( )
A.150mLB.200mLC.700mLD.400mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴蓝(化学式Al2CoO4)是一种耐热、耐光、耐酸、耐碱腐蚀的蓝色颜料。某企业利用含铝锂钴废料(铝箱、CoO和Co2O3、Li2O)制备钴蓝的工艺流程如下:
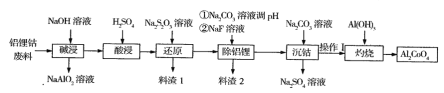
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是______,操作I的内容是_______。
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因___。
(3)写出“还原”过程中反应的离子方程式____。
(4)料渣2的主要成分是A1(OH)3 、____,写出灼烧时反应的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com