
已知A元素位于元素周期表第三周期,其原子最外层电子数是最内层电子数的一半。甲、乙、丙、丁四种物质均含有A元素,其中乙为白色固体,它们之间的相互转化关系如下图所示,试回答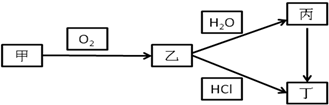
(1)A的元素符号为 ,丁的电子式为
(2)写出乙转化为丙的化学方程式
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| A | A是周期表中原子半径最小的元素 |
| B | B元素的原子价电子排布为ns1np4 |
| C | C的基态原子L层电子数是K层电子数的3倍 |
| D | D是第三周期中第一电离能最小的元素 |
| E | E是地壳中含量最多的金属元素 |
| F | 有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
查看答案和解析>>
科目:高中化学 来源:2013届河南许昌鄢陵一高高二下学期期中考试化学试卷(解析版) 题型:选择题
已知X.Y元素同周期,且电负性X>Y,下列说法正确的是
A.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
B.在同一周期中X位于Y的左面
C.Y的气态氢化物的稳定性大于X的气态氢化物的稳定性
D.X与Y形成的化合物中,X显负价,Y显正价
查看答案和解析>>
科目:高中化学 来源:重庆市2010届高三下学期5月月考(理综化学部分) 题型:填空题
(15分)A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍。已知:①热稳定性:HmD>HmC;② 、
、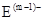 具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
(1)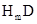 的电子式:_____________。
的电子式:_____________。
(2) 、
、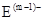 的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式______________________________。
(4)A和E形成的化合物,其晶体类型属___________;该晶体中离A最近的A有_____个。A和E形成化合物的熔点比C和E形成化合物的熔点_________(填高或低)。
(5)常温下,将等物质的量浓度的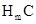 溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com