
【题目】某溶液中可能含有 Na+、K+、NH4+、Cu2+、SO42-、SO32-、MnO4-、Cl-、Br-、CO32-等离子,且所含离子的物质的量的浓度都相等。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成了如下实验:
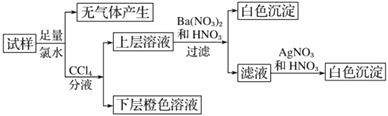
则关于原溶液组成的判断中正确的是:
A.肯定不存在的离子是 Cu2+、SO42-、CO32-、MnO4-,而是否含NH4+另需实验验证;
B.肯定存在的离子是SO32-、Br-,且Na+、K+至少有一种存在;
C.无法确定原溶液中是否存在Cl-;
D.若步骤中Ba(NO3)2和HNO3溶液改用 BaCl2和盐酸的混合溶液,对溶液中离子的判断无影响。
【答案】D
【解析】
往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成,则原溶液中无![]() ,加足量氯水,无气体,则无
,加足量氯水,无气体,则无![]() ,溶液加四氯化碳分液,下层橙色,则有Br-,上层加硝酸钡和稀硝酸有白色沉淀,有
,溶液加四氯化碳分液,下层橙色,则有Br-,上层加硝酸钡和稀硝酸有白色沉淀,有![]() ,因
,因![]() 与Cu2+能够发生相互促进的双水解反应,则原溶液中无Cu2+,因Br-、
与Cu2+能够发生相互促进的双水解反应,则原溶液中无Cu2+,因Br-、![]() 与
与![]() 能够发生氧化还原反应,因此原溶液中无
能够发生氧化还原反应,因此原溶液中无![]() ,溶液中一定含阳离子,且离子浓度都相等,根据电荷守恒,一定含有
,溶液中一定含阳离子,且离子浓度都相等,根据电荷守恒,一定含有![]() 、Na+、K+,一定不存在Cl-,滤液中加硝酸酸化的硝酸银有白色沉淀,是过程中加氯水时引入的氯离子。
、Na+、K+,一定不存在Cl-,滤液中加硝酸酸化的硝酸银有白色沉淀,是过程中加氯水时引入的氯离子。
A.分析可知肯定不存在的离子是Cu2+、![]() 、
、![]() 、Cl-、
、Cl-、![]() ,一定含
,一定含![]() ,故A错误;
,故A错误;
B.肯定存在的离子为:![]() 、
、![]() 、Br,根据溶液电中性可知原溶液中一定含有Na+、K+,故B错误;
、Br,根据溶液电中性可知原溶液中一定含有Na+、K+,故B错误;
C.根据电荷守恒,一定不存在Cl,故C错误;
D.加入Ba(NO3)2和HNO3溶液目的是检验硫酸根离子,因之前加入了氯水,氯水具有强氧化性,因此![]() 不会对检验硫酸根离子存在干扰,若改用BaCl2和盐酸的混合溶液,对溶液中离子的判断无影响,故D正确;
不会对检验硫酸根离子存在干扰,若改用BaCl2和盐酸的混合溶液,对溶液中离子的判断无影响,故D正确;
故答案为:D。


科目:高中化学 来源: 题型:
【题目】在恒温条件下,欲使CH3COONa的稀溶液中![]() 比值增大,可在溶液中加入少量下列物质中的( )
比值增大,可在溶液中加入少量下列物质中的( )
①固体NaOH ②固体KOH ③固体NaHSO4 ④固体CH3COONa ⑤冰醋酸
A.只有①②B.只有③⑤C.只有②④⑤D.只有①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2+O2(g)![]() 2SO3(g) △H<0,当反应达到平衡时,下列措施:
2SO3(g) △H<0,当反应达到平衡时,下列措施:
①降温 ②恒容通入惰性气体 ③增加SO2的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体 ⑦增大O2的浓度 ⑧将体积压缩到原来的一半,能提高SO2转化率的是( )
A.①②④B.④⑥⑦C.①⑦⑧D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液存在离子平衡,回答下列问题:
(1)Na2SO3水溶液呈________________(填“酸”、“中”、“碱”)性 ,原因是(用离子方程式):______________________________;
(2)已知T ℃时,纯水中c(OH)为10-6 mol·L-1,则
①该温度时0.1mol·L-1NaOH溶液pH为___________________。
②该温度下,将pH=2 的H2SO4溶液与pH=9的NaOH溶液按体积比1:9混合(忽略溶液体积变化),所得混合溶液的pH为________
③该温度下,若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性(忽略溶液体积变化),则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是___________。
(3)常温下,在25mL的氢氧化钠溶液中逐滴加入0.2mol·L-1醋酸溶液,滴定曲线如图所示。
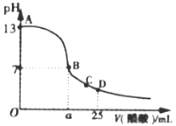
①在B点,溶液中n(CH3COO-)为______________________________。
②在D点,c(CH3COO) _________ c(Na+) (填“<”、“>”或“=”)。
③常温下将0.02mol CH3COONa和0.01mol盐酸溶于水,配成1L混合溶液。写出溶液中各离子浓度的大小关系为___________________________。
(4)常温下,在0.1mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液pH为8时,c(Cu2+)=________。(已知常温时Cu(OH)2的Ksp=2.2×10-20)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100 ℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示。下列说法中不正确的是( )
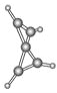
A. 该分子的分子式为C5H4
B. 该分子中碳原子的化学环境有2种
C. 该分子中的氢原子分布在两个相互垂直的平面上
D. 该分子中只有C—C键,没有![]() 键
键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿主要成分是 FeS2。某硫酸厂在进行黄铁矿成分测定时,取 0.1000 g 样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为 0.02000 mol·L-1的 K2Cr2O7标准溶液滴定至终点,重复实验,平均消耗K2Cr2O7标准溶液 20.00mL。
(1)硫酸工业中煅烧黄铁矿的设备名称_____。
(2)该样品FeS2的质量分数为_____;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯巴比妥是1903年就开始使用的安眠药,其合成路线如图(部分试剂和产物略)。
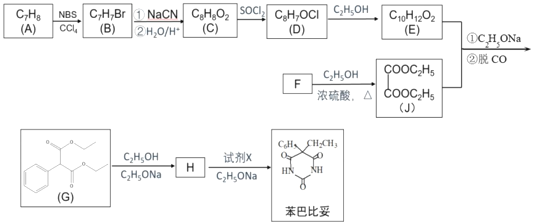
已知:①NBS是一种溴代试剂
②![]() +
+![]()
![]()
![]() + C2H5OH
+ C2H5OH
③R1—COOC2H5+![]()
![]()
![]() +C2H5OH
+C2H5OH
请回答下列问题:
(1)下列说法正确的是__________
A. 1 mol E在NaOH溶液中完全水解,需要消耗2 mol NaOH
B. 化合物C可以和FeCl3溶液发生显色反应
C. 苯巴比妥具有弱碱性
D. 试剂X可以是CO(NH2)2
(2)B中官能团的名称__________,化合物H的结构简式为_______。
(3)D→E的化学方程式为_________。
(4)苯巴比妥的一种同系物K,分子式为C10H8N2O3,写出K同时符合下列条件的同分异构体的结构简式______
①分子中含有两个六元环;且两个六元环结构和性质类似
②能够和FeCl3发生显色反应
③核磁共振氢谱显示分子中由5种氢
(5)参照流程图中的反应,设计以甲苯为原料合成聚酯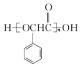 __________(用流程图表示,无机试剂任选)
__________(用流程图表示,无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡金属元素。A、B、C同周期,C、D同主族,A的原子结构示意图为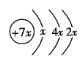 ,B的核外电子排布式为
,B的核外电子排布式为![]() ,C的最外层有三个单电子,E的价电子排布式为
,C的最外层有三个单电子,E的价电子排布式为![]() 。试回答下列问题:
。试回答下列问题:
(1)写出下列元素的符号:A______,B______,C______,D______。
(2)E元素原子的核电荷数是______,E元素在周期表中位于第______周期第______族;已知元素周期表可按电子排布分为![]() 区、
区、![]() 区、
区、![]() 区等,则E元素在______区。
区等,则E元素在______区。
(3)画出D的核外电子排布图:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍,A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73.2%和7.32%。
(1)A的分子式是__;
(2)已知:
ⅰ.![]() (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
ⅱ.![]()
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是__;
②若G为气体,且相对分子质量是44,则E的结构简式是__;E的核磁共振氢谱中有__个吸收峰(填数字);
③F→H的反应类型是__;
④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式__;
⑤A的结构简式是__;
上述转化中B→D的化学方程式是__;
(3)已知A的某种同分异构体K具有如下性质:
①K与FeCl3反应,溶液呈紫色
②K在一定条件下可发生银镜反应
③K分子中苯环上的取代基上无甲基
请写出K所有可能的结构简式__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com