
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24L三氯甲烷中含有的共价键数目为0.4NA
B. 常温常压下,7.8 g Na2O2中含有阴离子的数目为0.1NA
C. 1mol羟基与1mol氢氧根离子所含电子数均为9NA
D. 在1.0L 0.1 mol·L-1 Na2CO3溶液中,阴离子总数小于0.1NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】周期表中27号元素钴的方格中注明“3d74s2”,由此可以推断( )
A.它位于周期表的第四周期ⅡA族
B.它的基态核外电子排布式可简写为[Ar]4s2
C.Co2+的核外价电子排布式为3d54s2
D.Co位于周期表中第9列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷和红磷的着火点分别是40℃、240℃根据如图所示填空:
(1)铜片上燃烧;
(2)该实验证明,燃烧必须同时具备以下条件:①;②氧气(或空气);③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子的最外电子层上只有2个电子,该元素是
A. 一定是IIA元素 B. 一定是金属元素
C. 一定是正二价元素 D. 可能是金属元素,也可能是非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是 ( )
A. S2和S8的混合物共6.4g,其中所含硫原子数为0.2NA
B. 足量的铜片与含4molHNO3的浓硝酸充分反应生成的二氧化氮的分子数为2NA
C. 5.6g铁粉与硝酸反应失去的电子数一定为0.3 NA
D. 30g甲醛中含有的共用电子对数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图所示(部分产物已略去):
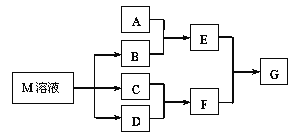
(1)写出用惰性电极电解M溶液的离子方程式____________。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是__________________。
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如下图所示,“则A与B溶液”反应后溶液中的溶质为__________(填化学式)。
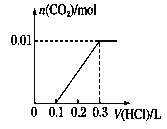
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是____________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是_______________ ;
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄露,请写出足量E与D反应的化学方程式___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com