
����Ŀ��������װ����ͼ���ӣ�D��F��X��Y��E ���Dz��缫��C�����缫���ף��ң�������װ���е��ǰ����Һ���������500mL������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ������˵������ȷ���ǣ������� 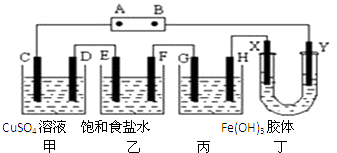
A.��ԴB ���������Ǹ���������Y��������ɫ����
B.��װ���е��һ��ʱ�����0.2mol��������Իָ�ԭ����Ũ��
C.��׳�����Һ������ڵ��ǰ����500ml�����ҳ���������������Ϊ4.48L����״����ʱ���׳������������ʵ����ʵ���Ũ��Ϊ0.2mol/L
D.��װ���е�ⷴӦ���ܻ�ѧ����ʽ�ǣ�CuSO4+Fe ![]() Cu+FeSO4
Cu+FeSO4
���𰸡�B
���������⣺A������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ��˵��F����NaOH���ɣ���FΪ������EΪ��������ԴAΪ������BΪ����������Y���ӵ�Դ��������YΪ������XΪ�����������������彺��������ɣ��������ƶ�����A��ȷ��
B�����е�ⷴӦ���ܻ�ѧ����ʽ�ǣ�2NaCl+2H2O ![]() H2��+Cl2��+2NaOH���൱������HCl���壬���ڷ�Ӧ�����ʵ��йؾ�����δ֪������ȷ������HCl���ʵ����������Ậ��ˮ����B����
H2��+Cl2��+2NaOH���൱������HCl���壬���ڷ�Ӧ�����ʵ��йؾ�����δ֪������ȷ������HCl���ʵ����������Ậ��ˮ����B����
C����װ���У�CΪ�������缫��ӦʽΪFe��2e��=Fe2+��DΪ�������缫��ӦʽΪ��Cu2++2e��=Cu����ⷴӦ���ܻ�ѧ����ʽ�ǣ�CuSO4+Fe ![]() Cu+FeSO4��
Cu+FeSO4��
���в�������Ϊ�������������������ʵ���֮��Ϊ1��1�����������ʵ���Ϊ ![]() ��
�� ![]() =0.1mol�����ݵ���ת���غ㣬��������FeSO4�����ʵ���Ϊ
=0.1mol�����ݵ���ת���غ㣬��������FeSO4�����ʵ���Ϊ ![]() =0.1mol��FeSO4�����ʵ���Ũ��Ϊ
=0.1mol��FeSO4�����ʵ���Ũ��Ϊ ![]() =0.2mol/L����C��ȷ��
=0.2mol/L����C��ȷ��
D����C�з�����֪����װ���е�ⷴӦ���ܻ�ѧ����ʽ�ǣ�CuSO4+Fe ![]() Cu+FeSO4����D��ȷ��
Cu+FeSO4����D��ȷ��
��ѡ��B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��BΪͬ�������Ԫ�أ�A��B����һ���ڣ���A��ԭ������Ϊn����B��ԭ������������Ϊ
A.n��8B.n��18C.n��20D.n��32
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F�����ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ���ǰ뾶��С��ԭ�ӣ�BԪ�ص�����������Ӧˮ����������̬�⻯�ﷴӦ����һ����X��D��Aͬ���壬����Fͬ���ڣ�FԪ�ص��������������������������3/4����A��B��D��F������Ԫ�أ�ÿһ����CԪ�ض����γ�Ԫ�ص�ԭ�Ӹ����Ȳ���ͬ�������ֻ����D��E��F����Ԫ�ض�Ӧ������������ˮ������������ܷ�Ӧ����ش��������⣺
��1��д��B��C��EԪ�ص�����B��C��E ��
��2��д��C��D����Ԫ���γɵ�ԭ�Ӹ�����Ϊ1��1�����ʵĵ���ʽΪ ��
��3��������֤C��F����Ԫ�طǽ�����ǿ���Ľ����ǣ����ţ��� �ٱȽ�������Ԫ�س������ʵ��۵�
�ڱȽ�������Ԫ�صĵ������������ϵ����׳̶�
�۱Ƚ�������Ԫ�ص���̬�⻯��Ļ�ԭ��
��4��A��C��D��F����Ԫ�ؿ����γ�������ʽ�Σ���������Ԫ����ɣ�����������ʽ�εĻ�ѧʽ�ֱ�Ϊ�� �� ��������ʽ�����Ӧ�����ӷ���ʽΪ ��
��5��A��C��F����γɼס��������������Ǿ�Ϊ��һ��˫ԭ�������ӣ��Ҽ���18�����ӣ�����10�����ӣ�������ҷ�Ӧ�����ӷ���ʽΪ ��
��6������a mol E���Ȼ������Һ�м��뺬b mol D������������Ӧˮ�������Һ�����ɳ��������ʵ���������Ϊ �� ��a mol ��b mol �� ![]() mol ��
mol �� ![]() mol ��0 �ޣ�4a��b��mol��
mol ��0 �ޣ�4a��b��mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������θ������صIJ��ˣ����ʺ�ʹ�õ�������� (����)
A.Mg(OH)2
B.Al(OH)3
C.NaHCO3
D.Na3C6H5O7��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������Ԫ�ص�ԭ�����������ƶ�ԭ�ӵĢ����������������������������������ܺ˵�������ݺ����������( )
A. �٢ڢۢ�B. �٢ڢܢ�C. �ڢۢܢ�D. �٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᣨ�Ҷ��ᣩ��������Ȼ���ֲ���У���K1=5.4��10��2 �� K2=5.4��10��5 �� ��������κͼ���������ˮ���������������ˮ�����ᾧ�壨H2C2O42H2O����ɫ���۵�Ϊ101�棬������ˮ��������ˮ��������170�����Ϸֽ⣮�ش��������⣺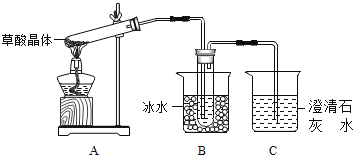
��1������ͬѧ������ͼ��ʾ��װ�ã�ͨ��ʵ�������ᾧ��ķֽ���װ��C�пɹ۲쵽�������� �� �ɴ˿�֪���ᾧ��ֽ�IJ������� �� װ��B����Ҫ������ ��
��2������ͬѧ��Ϊ���ᾧ��ֽ�IJ����к���CO��Ϊ������֤��ѡ�ü���ʵ���е�װ��A��B����ͼ��ʾ�IJ���װ�ã������ظ�ѡ�ã�����ʵ�飮 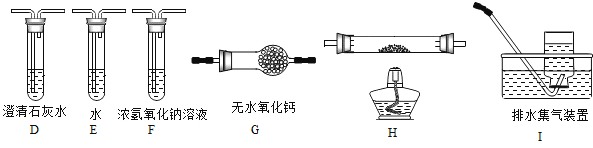
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��ΪA��B�� �� װ��H��Ӧ����ʢ�е������� ��
����֤�����ᾧ��ֽ��������CO�������� ��
��3�������ʵ��֤����
�ٲ�������Ա�̼���ǿ ��
�ڲ���Ϊ��Ԫ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1967��������������������ĸ���䶨��Ϊ��������仯����ӵ�����ֻ��������ϵĽ���Ԫ�أ���Cu9Al4��Cu5Zn8�ȣ��ش��������⣺ 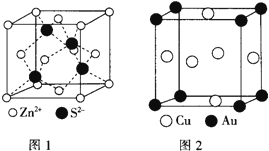
��1��ij�ֽ�������������Է��ԣ�ԭ������ά�ռ�����������������У��ý������������������ �塱�Ǿ��塱����
��2����̬ͭԭ������δ�ɶԵ��ӣ�����ͭ���ӵĵ����Ų�ʽΪ �� ��CuS04��Һ �е��������ˮ���γ���������ɫΪ ��
��3��ͭ������±�أ�SCN��2��Ӧ����Cu��SCN��2 �� 1mol��SCN��2�����к��У�������ĿΪ����±�أ�SCN��2��Ӧ���������֣������������ᣨH��S��C��N���ķе�����������ᣨH��N=C=S���ķе㣬��ԭ���� ��
��4��ZnS�ľ����ṹ��ͼ1��ʾ����ZnS�����У�S2������λ��Ϊ ��
��5��ͭ����γɵĽ���������ṹ��ͼ2���侧���߳�Ϊa nm���ý�����������ܶ�Ϊ���ú���a��NA �Ĵ���ʽ��ʾ��gcm��3 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ�����⣮���պϸ�װ�õĵ��ʱ���۲쵽�����Ƶ�ָ�뷢����ƫת����ش��������⣺ 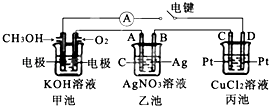
��1���׳���ͨ��CH3OH�缫�ĵ缫��ӦΪ ��
��2���ҳ���A��ʯī���缫������Ϊ������������������������������������������ҳ����ܷ�ӦʽΪ ��
��3�����ҳ���B����������5.40gʱ���׳�������������O2�����ΪmL����״���������������C����D����������gͭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ�Ļ�ѧ����ʽ����ע����1������2������3���ķ�Ӧ����
��1������ϩ�Ʊ�����ϩ�ķ�Ӧ��Ӧ���ͣ�
��2���üױ���TNT�ķ�Ӧ��Ӧ���ͣ�
��3����������NaOH���Ҵ���Һ������Ӧ���ͣ� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com