
| 编号 | I | II | III |
| 实验 | 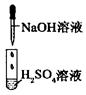 | 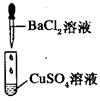 |  |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| ||
| ||
| 检验成分 | 操作步骤 | 实验现象与结论 |
| 铝 | 取少量固体样品加入NaOH溶液中 取少量固体样品加入NaOH溶液中 |
若有(无)气泡产生,说明该样品中含有(不含)铝 若有(无)气泡产生,说明该样品中含有(不含)铝 |
| 氧化铁 | 取少量样品加入稀硫酸中,滴加KSCN溶液 取少量样品加入稀硫酸中,滴加KSCN溶液 |
若溶液变红色,说明原样品中含有Fe2O3,反之,则不含Fe2O3 若溶液变红色,说明原样品中含有Fe2O3,反之,则不含Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 | 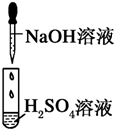 |
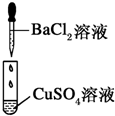 |
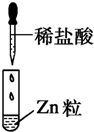 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省高一上学期期中考试化学试卷(解析版) 题型:选择题
某同学在实验室中进行如下实验:
|
编号 |
I |
II |
III |
|
实验 |
|
|
|
|
现象 |
没有明显变化,溶液仍为无色 |
有白色沉淀生成,溶液为蓝色 |
有无色气体放出 |
以下结论正确的是
A.I中混合前后溶液中各离子种类、个数均不变
B.II中反应前后溶液中Cu2+ 、Cl-浓度均未变
C.II中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同
D.III中发生的反应属于置换反应,不属于离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 | 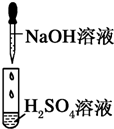 | 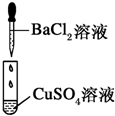 | 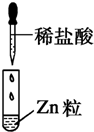 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省临沂市临沭实验中学高一(上)期中化学试卷(解析版) 题型:填空题
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 | 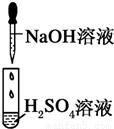 | 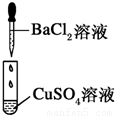 | 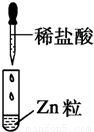 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com