
(15分)某兴趣小组的同学发现,将CuSO4溶液与Na2CO3溶液混合会产生蓝绿色沉淀。他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究。
Ⅰ.【提出猜想】
猜想1:所得沉淀为 ;
猜想2:所得沉淀为 ;
猜想3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2·nCuCO3]。
Ⅱ.【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
Ⅲ.【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
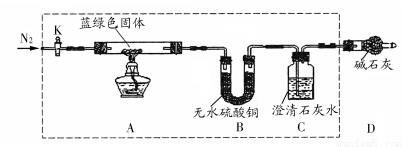
步骤2:取一定量所得固体,用如下装置(夹持仪器未画)进行定性实验;
Ⅳ.【问题讨论】
能证明猜想1成立的实验现象是 ;
(1)检查上述虚线框内装置气密性的实验操作是:关闭K, ;
(2)若在上述装置B中盛放无水CaCl2,C中盛放Ba(OH)2溶液,还可以测定所得沉淀的组成。
①C中盛放Ba(OH)2溶液,而不使用澄清石灰水的原因是 ;
②若所取蓝绿色固体质量为27.1 g,实验结束后,装置B的质量增加2.7 g,C中产生沉淀的质量为19.7 g 。则该蓝绿色固体的化学式为 。
(15分)
Ⅰ.猜想1:Cu(OH)2 ; (2分) 猜想2:CuCO3 ; (2分)
Ⅳ.现象:B中白色固体变蓝,C中无明显现象;(2分)
(若猜想1为CuCO3,则现象为:B中无明显现象,C中产生白色沉淀。)
(1)用酒精灯微热横玻璃管,若C中有气泡逸出,撤灯冷却一段时间,C中导管内形成水柱,则证明此装置气密性良好;(3分)
(2)① Ba(OH)2溶解度大于Ca(OH)2 ,能充分吸收CO2 ;(2分)且M(BaCO3)大于
M(CaCO3),测量误差小;(2分)
② Cu5(OH)6(CO3)2 (或:2CuCO3????3Cu(OH)2 )。(2分)
【解析】
试题分析:Ⅰ.根据Cu元素可能生成的沉淀的形式猜想。所得沉淀可能是Cu(OH)2或者是 CuCO3 ;
Ⅳ.如果沉淀是氢氧化铜,则受热分解生成氧化铜和水,无水硫酸铜与水结合生成蓝色固体,则B中白色固体变蓝,C中无明显现象;若沉淀是碳酸铜,则受热分解生成氧化铜和二氧化碳,二氧化碳使澄清石灰水变浑浊,则对应现象是B中无明显现象,C中产生白色沉淀。
(1)装置气密性的检查依据气体的压强原理,容器体积不变时,温度升高,压强增大。所以检查上述虚线框内装置气密性的实验操作是:用酒精灯微热横玻璃管,若C中有气泡逸出,撤灯冷却一段时间,C中导管内形成水柱,则证明此装置气密性良好;
(2)①若在上述装置B中盛放无水CaCl2,C中盛放Ba(OH)2溶液,则根据装置增重的质量来测定沉淀的组成。C中盛放Ba(OH)2溶液,Ba(OH)2溶解度大于Ca(OH)2 ,能充分吸收CO2 ;且M(BaCO3)大于M(CaCO3),测量误差小;
②装置B的质量增加2.7 g,C中产生沉淀的质量为19.7 g 。,说明27.1g的沉淀分解生成0.15g H2O,0.1mol CO2,则CuO的质量是4.7g,物质的量是0.25mol,所以沉淀中n(Cu):n(OH-):n(CO32-)=0.25:0.3:0.1=5:6:2,所以该沉淀的化学式为Cu5(OH)6(CO3)2.
考点:考查对实验的分析,装置气密性的检查,试剂的选择,化学式的计算


科目:高中化学 来源:2013-2014吉林松原市高一下学期期末化学试卷(解析版) 题型:选择题
关于化学键的各种叙述中正确的是( )
A.在离子化合物里,只存在离子键 B.非极性键只存在于双原子的单质分子里
C.共价化合物里,一定不存在离子键 D.不同元素组成的多原子分子里,只存在极性键
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林市高一化学下学期期末教学质量检测试卷(解析版) 题型:选择题
下列化学式只表示一种纯净物的是
A.C2H6 B.C2H4Cl2 C.C5H12 D.C
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林市高一化学下学期期末教学质量检测试卷(解析版) 题型:选择题
下列关系中,正确的是
A.原子半径:Mg>K B.非金属性:O<S
C.稳定性:HCl>HBr D.碱性:NaOH>KOH
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市通州区高考二模理综化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.生成物总能量一定低于反应物总能量
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的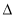 H不同
H不同
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g)
2NH3(g) 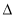 H =-38.6 kJ/mol
H =-38.6 kJ/mol
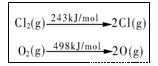
D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 mol
O2 反应放出115.6 kJ热量,键能如下表所示,则断裂1 mol
H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:实验题
(13分)
利用某含铬废液[含较低浓度的Na2Cr2O7、Fe2(SO4)3]制备K2Cr2O7。
流程如下:
Ⅰ.用NaOH溶液调pH至3.6,产生红褐色沉淀,过滤;
Ⅱ.向滤液中加入Na2SO3,一定操作后分离出Na2SO4;
Ⅲ.将分离出Na2SO4后的溶液调pH约为5,得到Cr(OH)3沉淀;
Ⅳ.在KOH存在条件下,向Cr(OH)3中加入足量H2O2溶液,得到黄色溶液;
Ⅴ.向黄色溶液中加入物质A后,溶液变为橙红色,一定操作后得到K2Cr2O7固体;
Ⅵ.测定K2Cr2O7固体的纯度。
已知:Cr2O72-(橙红色)+H2O 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+
(1)步骤Ⅰ中红褐色沉淀的化学式是 。
(2)步骤Ⅱ中加入Na2SO3的目的是 。
(3)步骤Ⅳ中反应的离子方程式是 。
(4)步骤Ⅴ中加入的物质A可以是 。(填序号)
a.KOH b.K2CO3 c.H2SO4 d.SO2
(5)步骤Ⅵ的操作是:取0.45 g K2Cr2O7产品配成溶液,酸化后滴入18.00 mL
0.50 mol/L的FeSO4溶液,恰好使Cr2O72-完全转化为Cr3+。产品中K2Cr2O7的纯度是 。(注:K2Cr2O7的摩尔质量为294 g/mol)
(6)向橙红色的K2Cr2O7溶液中,滴加Ba(NO3)2溶液,产生黄色沉淀,溶液pH减小。试推测黄色沉淀是 ,溶液pH变小的原因是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区下学期高二年级期末考试化学试卷(解析版) 题型:填空题
(4分)有机物具有广泛的用途。现有下列有机物:①乙烯 ②1,3-丁二烯 ③甲醛 ④油脂。请将相应的序号填入空格内。
(1)能用于制备肥皂的是____________; (2)能用于制备聚乙烯塑料的是____________;
(3)能用于制备顺丁橡胶的是____________; (4)能用于制备酚醛树脂的是____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区下学期高一年级期末考试化学试卷(解析版) 题型:选择题
某化学反应中,反应物B的物质的量浓度在20s内,从2.0mol/L变成了1.0mol/L,则这20s内B的反应速率为
A.0.05mol/(L s) B.0.05 C.0.5mol/(L
s) B.0.05 C.0.5mol/(L s) D.0.05mol/L
s) D.0.05mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com