


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液的物质的量浓度为1mol/L |
| B、该溶液中含有35.5g Na2SO4 |
| C、配制1 00ml该溶液需用7.1g Na2SO4 |
| D、量取100ml该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、原子结构示意图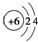 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
B、比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
C、结构示意图为 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D、电子式 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在熔化状态下能导电的化合物为离子化合物 |
| B、根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸 |
| C、CO2、SiO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2为碱性氧化物 |
| D、因为Na2O的水溶液能导电,所以Na2O是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+ Mg2+ Al3+ Ba2+ Fe3+ | ||||
| 阴离子 | OH- Cl- C
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com