
下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质:
试样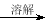
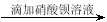 白色沉淀
白色沉淀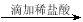 沉淀不溶解→说明试样已变质
沉淀不溶解→说明试样已变质
B.除去粗盐中含有的硫酸钙杂质:
粗盐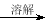

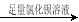
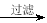
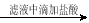
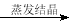 精盐
精盐
C.检验某溶液中是否含有Fe2+:
试样 溶液颜色无变化
溶液颜色无变化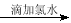 溶液变红色→溶液中含有Fe2+
溶液变红色→溶液中含有Fe2+
D.证明酸性条件H2O2的氧化性比I2强:
NaI溶液
 溶液变紫色→氧化性:H2O2>I2
溶液变紫色→氧化性:H2O2>I2
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.NaClO溶液中:c(Na+)=c(ClO-)+c(OH-)+c(HClO)
B.常温下,pH=a的NH4Cl溶液中由水电离产生的c(OH-)=10-amol·L-1
C.向0.1 mol·L-1的Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
D.Na2S稀溶液中:c(OH-)=c(H+)+2c(H2S)+c(HS-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:实验题
(1)配制100 mL 0.10 mol·L-1NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→___ ___(冷却后)→洗涤(并将洗涤液移入容量瓶)→___ ___→___ ___→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量________g氢氧化钠固体所需仪器有:托盘天平(带砝码、镊子)、________、________。
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用已配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是___________________________________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为_____________(保留两位有效数字)。
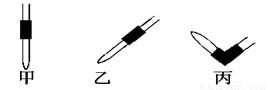
③排去碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
A.滴定终点读数时俯视
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
在体积可变的密闭容器中,反应m A (g)+n B (s) 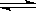 p C (g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是
p C (g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是
A.(m+n)必定小于p B.(m+n)必定大于p
C.m必定 小于p D.n必定大于
小于p D.n必定大于 p
p
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上第三次调研化学试卷(解析版) 题型:实验题
[有机化学基础]H是一种香料的成分之一,其结构中含有三个六元环。G的结构简式为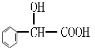 ,H的合成路线如下(部分产物和反应条件略去):
,H的合成路线如下(部分产物和反应条件略去):
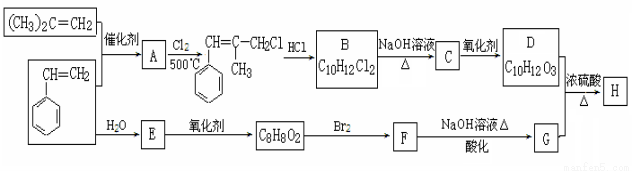
已知:① B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
②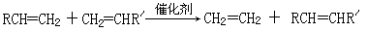
③D和G是同系物
(1)用系统命名法命名(CH3)2C=CH2 。
(2)A→B反应过程中涉及的反应类型有 。
(3)G分子中含氧官能团的名称: 。
(4)写出B与足量氢氧化钠溶液在加热条件下反应的化学方程式: 。
(5)写出F的结构简式: 。
(6)同时满足下列3个条件:①与FeCl3溶液发生显色反应;②能发生水解反应;③苯环上有两个取代基的G的同分异构体有 种(不包括立体异构),其中核磁共振氢谱为5组峰的为 (写结构简式)
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上第三次调研化学试卷(解析版) 题型:选择题
下列实验的现象与对应结论均正确的是( )
选项 | 操 作 | 现 象 | 结论 |
A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸只表现脱水性 |
B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
D | 将盐酸滴入Na2CO3溶液中 | 产生气泡 | Cl的非金属性比C强 |
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次段考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,X的一种核素在考古时常用来鉴定文物年代,Z的单质在空气中的燃烧产物与水反应有Y单质产生,W2、WY2可用于自来水消毒。下列说法正确的是( )
A. 原子半径大小:Z<X B. 氢化物的稳定性:X>W
C. ZWY3是含有离子键的共价化合物 D. 氢化物的沸点:Y>W
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考二化学卷(解析版) 题型:实验题
【化学 — 有机化学基础】3-对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
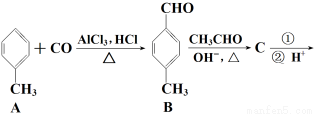
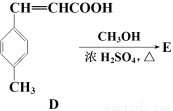
已知:HCHO+CH3CHO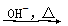 CH2===CHCHO+H2O
CH2===CHCHO+H2O
(1) A的核磁共振氢谱图显示峰的面积比为_________;A→B新生成的官能团名称为 。
(2) B的同系物G(C9H10O)的同分异构体有多种,其中满足下列条件的同分异构体数目有 种(不考虑立体异构)① 遇FeCl3溶液呈紫色;②苯环上有两个取代基。
(3) C的结构简式为___________;D→E的反应类型为___________。
(4) 过程①选用的试剂可选用下列中的___________。
a.溴水 b. 银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(5) 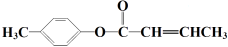 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________。
(6) E在一定条件下可以合成高聚物F,F的结构简式为___________。
查看答案和解析>>
科目:高中化学 来源:2017届广东省肇庆市高三上学期二模化学试卷(解析版) 题型:填空题
为了有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物含量、使用清洁能源显得尤为重要。
(1)已知:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ∆H = -905.48 kJ·mol-1
4NO(g)+6H2O(g) ∆H = -905.48 kJ·mol-1
N2(g)+O2(g) 2NO(g) ∆H = +180.50 kJ·mol-1
2NO(g) ∆H = +180.50 kJ·mol-1
则4NH3(g)+6NO(g) 5N2(g)+6H2O(g)的∆H = 。
5N2(g)+6H2O(g)的∆H = 。
(2)某化学小组查阅资料知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) N2O2(g) (快) ∆H1<0 v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
N2O2(g) (快) ∆H1<0 v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) 2NO2(g) (慢) ∆H2< 0
2NO2(g) (慢) ∆H2< 0
v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
① 2NO(g)+O2(g) 2NO2(g)的反应速率主要是由_______(填“第一步”或“第二步”)反应决定。
2NO2(g)的反应速率主要是由_______(填“第一步”或“第二步”)反应决定。
② 一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K= ;升高温度,K值 (填“增大”、“减 小”或“不变”)
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K= ;升高温度,K值 (填“增大”、“减 小”或“不变”)
(3)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g) N2(g)+xCO2(g) △H <0;理论上,适当增加汽车排气管(内壁为活性炭涂层)长度______(填“能”或“不能”)使NOx更加有效地转化为无毒尾气而排放,其原因是 。
N2(g)+xCO2(g) △H <0;理论上,适当增加汽车排气管(内壁为活性炭涂层)长度______(填“能”或“不能”)使NOx更加有效地转化为无毒尾气而排放,其原因是 。
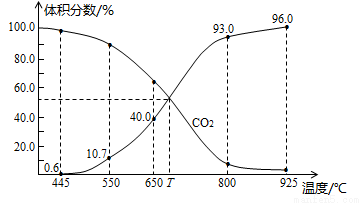
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应: C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示,则800℃时,反应达平衡时CO2的转化率为________(保留一位小数)。
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示,则800℃时,反应达平衡时CO2的转化率为________(保留一位小数)。
(5)氢气是一种重要的清洁能源,Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com