
��12�֣���Ԫ�صĵ��ʺͻ������ڹ���ũҵ��������;�㷺��������β���к���NO�ȶ�����Ⱦ�
��1��������ʳƷ������������� ��(�ѧʽ)������������Ļ������� ��(�ѧʽ)�������ڿ�������HCl�����а���������������Ļ�ѧ��Ӧ����ʽ�� ��
��2�������ũҵ�ϴ���������ʡ�ʵ���ҿ��ù������NH4Cl�����Ca(OH)2���ȷ�Ӧ���Ʊ��������仯ѧ����ʽΪ ��
��3������ȼ����һ�㲻����Ԫ�أ���β��ȴ������NO��������ԭ���û�ѧ����ʽ��ʾ ��
��4��NO�Դ�����Ӱ��֮һ�ǵ������꣬�û�ѧ����ʽ��ʾNO�γ������ԭ���� ��
��1��N2��1�֣�NH3 ��1�֣� NH3 + HCl===NH4Cl��2�֣� ��2��2 NH4Cl+Ca(OH)2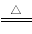 +CaCl2 +2 NH3��+2 H2O��2�֣� ��3��N2 +O2
+CaCl2 +2 NH3��+2 H2O��2�֣� ��3��N2 +O2  2NO ��2�֣� ��4��2NO + O2 === 2NO2 ��2�֣� 3NO2 + H2O === 2HNO3 +NO ��2�֣�
2NO ��2�֣� ��4��2NO + O2 === 2NO2 ��2�֣� 3NO2 + H2O === 2HNO3 +NO ��2�֣�
��������
�����������1��������ʳƷ�ı��������ǵ�������ѧʽ��N2������Һ̬NH3�������մ������ȣ��������������NH3��HCl��Ӧ�Ļ�ѧ����ʽΪ��NH3 + HCl===NH4Cl����2��NH4Cl�����Ca(OH)2���ȷ�Ӧ���Ʊ���������ѧ����ʽΪ��2 NH4Cl+Ca(OH)2 CaCl2 +2 NH3��+2 H2O����3������β���е�NO��N2��������O2��Ӧ���ɣ���ѧ����ʽΪ��N2 +O2
CaCl2 +2 NH3��+2 H2O����3������β���е�NO��N2��������O2��Ӧ���ɣ���ѧ����ʽΪ��N2 +O2  2NO����4��NO����������Ҫ������NO������е�O2��Ӧ������NO2��NO2��ˮ��Ӧ����HNO3����Ӧ�Ļ�ѧ����ʽΪ��2NO + O2 === 2NO2 �� 3NO2 + H2O === 2HNO3 +NO
2NO����4��NO����������Ҫ������NO������е�O2��Ӧ������NO2��NO2��ˮ��Ӧ����HNO3����Ӧ�Ļ�ѧ����ʽΪ��2NO + O2 === 2NO2 �� 3NO2 + H2O === 2HNO3 +NO
���㣺�����仯��������ʡ���������ȡ��������γɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и����������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ��ȷ����
A. CO2�ı���ģ�ͣ�
B. �����ӵĽṹʾ��ͼ��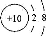
C. ������Ľṹʽ��
D. ���ĵ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������һ�����У��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�����������˵����ȷ����
A����ͬ��ͬѹʱ����ͬ������κ�����������ԭ����Ŀ��ͬ
B����49g H2SO4����1Lˮ�У�������Һ�����ʵ���Ũ��Ϊ0.5molL-1
C����״���£�11.2Lˮ����������Ϊ0.5 NA
D�������£�2.7g�������������ᷴӦ��ʧȥ�ĵ�����Ϊ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������һ�����У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һһ�������Ե���
A��c (H+) �� c(OH-) =10-14����Һ
B��n(H+)=n(OH��) ����Һ
C��c (H+)=1.0��10-7 mol/L����Һ
D��pH=3������pH=11�ļ�������Ϻ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������һ�����У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��������������ǿ����ʵ���
A��NH3��H2O B��Cl2 C��NaCl��Һ D��NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�Ϫ�ظ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�����,����������ȷ����
A��18gˮ�������ĵ�����Ϊ8NA
B��11.2L���������ķ�����Ϊ0.5NA
C��2.4gMg�����������ᷴӦʧȥ�ĵ�����Ϊ0.2NA
D��32g��������������ԭ����ΪN
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�Ϫ�ظ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�۲춡����������ȷ������
A���۲������������佺����һ����ƽ��
B����һ����İ׳������ʢ�н�����ձ����Ϸ�
C���۲������ߴ�ֱ��һ������⣬�����ð�����
D���������������������۲������������佺���ڵĺ�ɫ���ⴹֱ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�Ϫ�ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������������(K2FeO4)�Ѿ����㷺Ӧ����ˮ�������棬������ص������Գ���������أ���һ�ּ����������������ۡ�ɱ��������Ч�Ķ��ˮ�����������������ˮ�����������漰���Ĺ�����ȷ����
�ٵ����ʵı��� �ڵ����ʵ����� �۽���۳� ������ˮ��
����ɫ��Ӧ ��������ԭ��Ӧ
A���٢ڢۢ� B���٢ۢܢ� C���ڢۢܢ� D���ڢۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ��̨�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣��������������������������Դ�������ʣ���Ч���ٻ�����Ⱦ��ij�������Ž��ѵ��������ȼҵ���״�������������������Ҫ�������£�

��1����ҵ��ⱥ��ʳ��ˮ�Ļ�ѧ����ʽΪ________������������Ϊ________���ѧʽ����
��2�����������������������ڸ��������¾����Ȼ����õ����Ȼ��ѵĻ�ѧ����ʽΪ________��
��3����֪���� Mg(s) + Cl2(g) = MgCl2(s) ��H = -641 kJ��mol-1
�� Ti(s) + 2Cl2(g) = TiCl4(s) ��H = -770 kJ��mol-1
�� 2Mg(s) + TiCl4(g) = MgCl2(s) + Ti(s) ��H = ________��
��4����25�桢101kPa�����£�1 gҺ̬�״�(CH3OH)ȼ������CO2��Һ̬ˮʱ����22.7 kJ�����ʾ�״�ȼ�յ��Ȼ�ѧ����ʽΪ��________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com