
| A. | 高纯硅广泛应用于太阳能电池、计算机芯片和半导体器件的制造 | |
| B. | 煤炭经气化、液化和干馏等过程,可以转化为清洁燃料和化工原料 | |
| C. | PM2.5是指直径接近2.5×10-6m的颗粒物分散在空气中形成的污染物的胶体 | |
| D. | 门捷列夫在前人的基础上发现了元素周期律,表明科学研究既要继承又要创新 |
分析 A.高纯硅是优良的半导体材料;
B.煤炭经气化、液化和干馏可剔除一些污染物的排放,可获得清洁能源和重要的化工原料;
C.胶体的分散系中分散质的直径在1~100nm;
D.门捷列夫发现元素周期律并编制出元素周期表.
解答 解:A.高纯硅是优良的半导体材料,广泛应用于太阳能电池、计算机芯片,故A正确;
B.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或者利用煤产生的H2和CO通过化学合成产生液体燃料或者其他液体化工产品的过程;煤的干馏是指隔绝空气加强热,使煤分解的过程,可以得到很多重要的化工原料,故B正确;
C.胶体的分散系中分散质的直径在1~100nm,PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,直径大于100nm,则细颗粒物分散在空气中形成的分散系不是胶体,故C错误;
D.1865年门捷列夫发现元素周期律并编制出元素周期表,表明科学研究既要继承又要创新,使化学的学习有了理论指导,故D正确;
故选C.
点评 本题考查内容较多,涉及高纯硅用途、煤的加工、胶体、元素周期律发现等知识,侧重于基础知识的考查,注意相关基础知识的积累,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
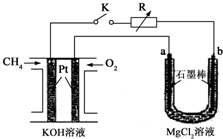 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每一个水分子内含有两个氢键 | |
| B. | 水分子的空间构型为V形 | |
| C. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| D. | 水是良好的溶剂,易溶解HCl、CH4等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
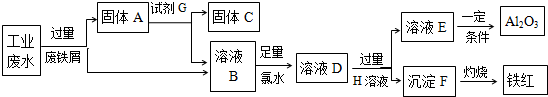
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象 | 解释 |
| A | Cl2在H2中点燃,瓶口有白雾 | 生成HCl极易溶于水 |
| B | 饱和Na2CO3溶液中通入CO2析出白色晶体 | 生成NaHCO3溶解度小析出 |
| C | 常温下将铝片放入浓硝酸中无明显变化 | Al和浓硝酸不反应 |
| D | SO2通入溴水,溴水褪色 | SO2具有还原性. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向无色溶液中滴加氯水和CCl4,振荡静置 | 下层溶液显紫色 | 溶液中含有I- |
| B | 过量铁粉加入稀硝酸中充分反应,再加入 KSCN溶液 | 溶液呈红色 | 稀硝酸将铁氧化为Fe3+ |
| C | 向BaC12溶液中先通入SO2 | 生成白色沉淀 | 白色沉淀是BaSO4 |
| D | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸先变红后变黑 | 浓硫酸具有酸性和脱水性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水加入溴化钠溶液中 | B. | 溴水加入氟化钠溶液中 | ||
| C. | 氯水加入碘化钾溶液中 | D. | 溴水加入碘化钾溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com