
| A. | 在反应 KClO3+6HCl═KCl+3Cl2↑+3H2O 中,Cl2既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA | |
| B. | 标准状况下,22.4 L 甲苯中含有的 C-H 键数目为 8NA | |
| C. | 50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA | |
| D. | t℃时,MgCO3的 Ksp=4×10-6,则该温度下饱和 MgCO3溶液中含有的 Mg2+数目为 2×10-3 NA |
分析 A、反应 KClO3+6HCl═KCl+3Cl2↑+3H2O 转移5mol电子,生成3mol氯气;
B、标况下,甲苯为液体;
C、在乙醇的水溶液中,除了乙醇外,水也含H原子;
D、溶液体积不明确.
解答 解:A、反应 KClO3+6HCl═KCl+3Cl2↑+3H2O 转移5mol电子,生成3mol氯气,故当生成标况下67.2L即3mol氯气时,转移5NA个电子,故A正确;
B、标况下,甲苯为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、在乙醇的水溶液中,除了乙醇外,水也含H原子,故此溶液中的H原子总数大于3NA个,故C错误;
D、溶液体积不明确,故饱和的碳酸镁溶液中的镁离子的个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
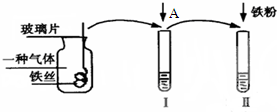 如图是某次实验探究铁及其化合物性质的流程图:
如图是某次实验探究铁及其化合物性质的流程图:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
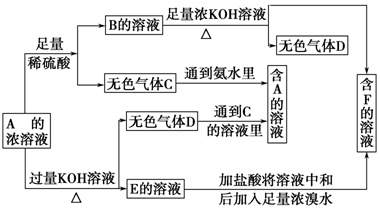
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 16g O2中所含的氧原子数为NA | |
| C. | 标准状况下,22.4L水中含有NA个水分子 | |
| D. | 标准状况下,22.4L氯化氢所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 氧化物 | 环境问题 | 主要来源 | |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | CO | CO中毒 | 汽车尾气和化石燃料的不完全燃烧 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{b}{11.2V}$ | B. | p=m+$\frac{{V}_{c}}{125}$ | C. | n=m+17Vc | D. | $\frac{17}{9}$m<p<$\frac{5}{3}$m |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
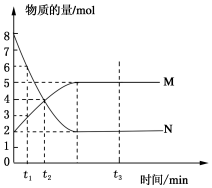 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com