
| b�Ma��ȡֵ��Χ | ���� | �������ʵ��� |
���� ��1�����ݼ������з�����0��$\frac{b}{a}$��$\frac{5}{4}$���������㣬������Ӧ��4NH3+5O2=4NO+6H2O��Ȼ��������ʺ������ʵ�����
$\frac{b}{a}$=$\frac{5}{4}$��ǡ�÷�Ӧ��������Ӧ��4NH3+5O2=4NO+6H2O��NO������ˮ��Ҳ����ˮ��Ӧ��
$\frac{5}{4}$��$\frac{b}{a}$��2���ȷ�����Ӧ��4NH3+5O2=4NO+6H2O��Ȼ������Ӧ��4NO+3O2+2H2O��4HNO3��O2���㣬Ȼ��������ʺ������ʵ�����
$\frac{b}{a}$��2 ������Ӧ��4NH3+8O2=4HNO3+4H2O��O2������Ȼ��������ʺ������ʵ�����
��2�������$\frac{b}{a}$��Ȼ����ݣ�1���жϲ��Ȼ��ó���Һ��������ϲ����ܶȼ������Һ�����������������������������ʵ���Ũ�ȣ�
��� �⣺��1�����ݼ������з�����0��b�Ma��5�M4��O2���㣬������Ӧ��4NH3+5O2=4NO+6H2O������ΪNH3���μӷ�Ӧ��NH3�����ʵ���Ϊ��$\frac{4b}{5}$mol��ʣ���NH3�����ʵ���Ϊ��a-$\frac{4b}{5}$��mol��
$\frac{b}{a}$=$\frac{5}{4}$��ǡ�÷�Ӧ��������Ӧ��4NH3+5O2=4NO+6H2O��NO������ˮ��Ҳ����ˮ��Ӧ��������Һ�������ʣ�
$\frac{5}{4}$��$\frac{b}{a}$��2���ȷ���4NH3+5O2=4NO+6H2O������NOamol������O2Ϊ��$\frac{5}{4}$amol��Ȼ������Ӧ��4NO+3O2+2H2O��4HNO3��O2���㣬����ΪHNO3���μӷ�Ӧ�����������ʵ���bmol-$\frac{5}{4}$amol�����ɵ�HNO3Ϊ��bmol-$\frac{5}{4}$amol����$\frac{4}{3}$=$\frac{4b-5a}{3}$mol��
$\frac{b}{a}$��2 ������Ӧ��4NH3+8O2=4HNO3+4H2O��O2����������ΪHNO3�������ʵ���Ϊamol��
�ʴ�Ϊ��
| b�Ma��ȡֵ��Χ | ���� | �������ʵ��� |
| 0��$\frac{b}{a}$��$\frac{5}{4}$ | NH3 | ��a-$\frac{4b}{5}$��mol |
| $\frac{b}{a}$=$\frac{5}{4}$ | / | / |
| $\frac{5}{4}$��$\frac{b}{a}$��2 | HNO3 | $\frac{4b-5a}{3}$mol |
| $\frac{b}{a}$��2 | HNO3 | amol |
���� ������Ҫ���췴Ӧ��Ķ��ٶԷ�Ӧ��Ӱ��ͻ������㹫ʽ������ʹ�ã���Ŀ�ѶȽϴ���ȷ������Ӧ��ʵ��Ϊ���ؼ���ע�������������ʵ��������ʵ���Ũ�ȡ�Ħ��������֮��Ĺ�ϵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
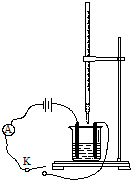 ��ͼ�����ʽ�ζ��ܺ��ձ��зֱ�ע��0.2mol•L-1Ba��OH��2��Һ��0.1mol•L-1ϡ�����50mL������ϡ�����еμӼ���ʯ����Һ������ͼװ�����Ӻã�
��ͼ�����ʽ�ζ��ܺ��ձ��зֱ�ע��0.2mol•L-1Ba��OH��2��Һ��0.1mol•L-1ϡ�����50mL������ϡ�����еμӼ���ʯ����Һ������ͼװ�����Ӻã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ����˫��ˮΪԭ��������������������д���ϳɹ������������Ļ�ѧ��Ӧ����ʽ��
����˫��ˮΪԭ��������������������д���ϳɹ������������Ļ�ѧ��Ӧ����ʽ�� ��
��
 �����ڷ���ṹ��ͬ���칹����3�֣�
�����ڷ���ṹ��ͬ���칹����3�֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڳ�ʪ�Ŀ����з��ò������� | B�� | Ӳ�ȱ������� | ||
| C�� | ��2mol/L����ķ�Ӧ�������� | D�� | �����ŨH2SO4��Һ�пɶۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Li��������ȼ����Ҫ����Li2O | |
| B�� | ±��Ԫ�ص���X2��X������F��Cl��Br��I����������ˮ��Ӧ����HX | |
| C�� | ��SO2ͨ����������Һ���ܵõ������� | |
| D�� | ��NH3ͨ���ȵ�CuSO4��Һ����ʹCu2+��ԭ��Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C14H18O5 | B�� | C14H16O4 | C�� | C14H22O5 | D�� | C14H10O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 64 g SO2������ԭ����ΪNA | |
| B�� | 1 mol��������ϡ���ᷴӦת�Ƶĵ�����ĿΪ3 NA | |
| C�� | ��ͬ��ͬѹ�£���ͬ������κ����嵥��Ӧ������ͬ��ԭ���� | |
| D�� | ���³�ѹ�£�14 g N2���з�����Ϊ0.5 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ܷ�����ȥ��Ӧ | B�� | ������Ϊͪ | ||
| C�� | ����Na��Ӧ | D�� | ���ܷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com