
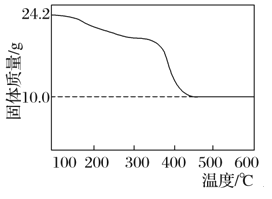
【题目】现有48.4 g碱式碳酸镁样品(化学式:xMgCO3·yMg(OH)2·zH2O,x、y、z为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入150 mL某浓度的盐酸中,充分反应后生成CO2 4.48 L(已折算成标准状况下),所得溶液稀释至250 mL,测得溶液的c(H+)=0.100 mol·L-1。
按要求回答下列问题:
(1)盐酸的物质的量浓度c(HCl)=________mol·L-1。
(2)x∶y∶z=________。
【答案】 3.50 )4∶1∶5
【解析】(1)24.2g样品与盐酸反应放出的二氧化碳的物质的量为![]() =0.2mol,即n(MgCO3)=0.2mol,将24.2g样品灼烧至恒重得到10.0g氧化镁,含有镁元素的物质的量为
=0.2mol,即n(MgCO3)=0.2mol,将24.2g样品灼烧至恒重得到10.0g氧化镁,含有镁元素的物质的量为![]() =0.25mol,则n[Mg(OH)2]=0.25mol-0.2mol=0.05mol,反应的盐酸的物质的量为0.2mol×2+0.05mol×2=0.5mol,溶液中剩余的氢离子的物质的量为0.100 mol·L-1×0.25L=0.025mol,因此盐酸中氯化氢的总量为0.5mol+0.025mol=0.525mol,则c(HCl)=
=0.25mol,则n[Mg(OH)2]=0.25mol-0.2mol=0.05mol,反应的盐酸的物质的量为0.2mol×2+0.05mol×2=0.5mol,溶液中剩余的氢离子的物质的量为0.100 mol·L-1×0.25L=0.025mol,因此盐酸中氯化氢的总量为0.5mol+0.025mol=0.525mol,则c(HCl)=![]() =3.50mol/L,故答案为:3.50;
=3.50mol/L,故答案为:3.50;
(2)根据题意,24.2g样品与盐酸反应放出的二氧化碳的物质的量为![]() =0.2mol,即n(MgCO3)=0.2mol,将24.2g样品灼烧至恒重得到10.0g氧化镁,含有镁元素的物质的量为
=0.2mol,即n(MgCO3)=0.2mol,将24.2g样品灼烧至恒重得到10.0g氧化镁,含有镁元素的物质的量为![]() =0.25mol,则n[Mg(OH)2]=0.25mol-0.2mol=0.05mol,含有结晶水的质量为24.2g-0.2mol×84g/mol-0.05mol×58g/mol=4.5g,物质的量为
=0.25mol,则n[Mg(OH)2]=0.25mol-0.2mol=0.05mol,含有结晶水的质量为24.2g-0.2mol×84g/mol-0.05mol×58g/mol=4.5g,物质的量为![]() =0.25mol,x∶y∶z=0.2mol:0.05mol:0.25mol=4∶1∶5。
=0.25mol,x∶y∶z=0.2mol:0.05mol:0.25mol=4∶1∶5。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】下列检验方法,利用该气体的氧化性的是
A. Cl2使湿润的淀粉碘化钾试纸变蓝
B. SO2使品红溶液褪色
C. NH3使湿润的红色石蕊试纸变蓝
D. NO遇到空气变为红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中,可大量共存的离子组是( )
A.Na+、CO32-、SO42-、Cl- B.Cu2+、NO3-、Cl-、SO42-
C.H+、Cl-、K+、CO32- D.K+、Mg2+、SO42-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟七号”的燃料是氢化锂三兄弟:LiH、LiD、LiT。其中Li的质量数为7,则对相同物质的量的这三种物质的下列说法正确的是( )
A. 质子数之比为1:2:3 B. 中子数之比为1:1:1
C. 摩尔质量之比为8:9:10 D. 化学性质不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。Fe(OH)3、Al(OH)3沉淀的生成与溶解的pH列于下表。(已知:偏铝酸钡易溶于水)。以下推断正确的是
氢氧化物 | 溶液pH | |||
开始沉淀 | 完全沉淀 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.1 | — | — |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
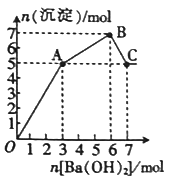
A. OA段产生的沉淀为:Fe(OH)3和Al(OH)3
B. AB段可能发生的反应是:Al3++3OH-=Al(OH)3↓
C. Al3+的物质的量浓度是2mol·L-1
D. C点沉淀的质量为806g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性。将水合肼通入CuO胶体中,可发生如图所示的转化。

(1)图示的转化中,②属于_____________(填“非氧化还原反应”或“氧化还原反应”)。
(2)转化①中,氧化剂与还原剂的物质的量之比为4: l ,则X的化学式为_____。
(3)转化②中,反应一段时间后,溶液中n(OH-)____________(填“增大”“ 减小” 或“不变”)。
(4)若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,则③中参加反应的O2的物质的量与④中今加反应的NaClO的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,分别向体积、浓度均为20mL0.1mol·L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示。(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
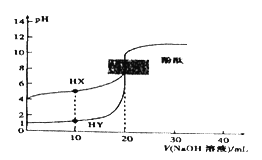
A. 298K 时,0.1mol·L-1HX 溶液中HX的电离度为1%
B. V=10mL时,同时微热溶液(忽略体积变化), 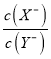 逐渐增大
逐渐增大
C. V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-)
D. 滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com