
| A. | SiH4的空间构型是正四面体 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 | |
| D. | SO2、SO3都是极性分子 |
分析 A.分子的空间构型是正四面体,所含中心原子应能形成4个σ键,且结构对称,中心原子所形成的共价键键长相等;
B.NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键,[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键;
C.原子晶体中原子以共价键结合,形成网状结构,具有键能大、熔点高、硬度大的特性;
D.对于ABn型分子,A原子的最外层电子,若完全成键,属于非极性分子,若不完全成键,则属于极性分子,SO2是极性分子,SO3分子是非极性分子.
解答 解:A.硅烷中Si原子形成4个Si-H键,共价键键长相等,结构对称,为正四面体结构,故A正确;
B.NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键,[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键,故B正确;
C.原子晶体中原子以共价键结合,形成网状结构,具有键能大、硬度大的特性,如二氧化硅、金刚石等原子晶体,故C正确;
D.SO2中S元素化合价为+4,S原子最外层6个电子未全部成键,为极性分子,SO3中S元素化合价为+6,S原子最外层6个电子全部成键,为非极性分子,故D错误;
故选D.
点评 本题考查了分子的空间构型、配位键、原子晶体性质特征、分子极性的判断等知识,题目难度不大,注意相关基础知识的积累.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:选择题
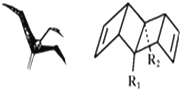 始祖鸟烯形状宛如一只展翅低头飞翔的鸟,其键线式结构表示如图,其中R 1、R 2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )
始祖鸟烯形状宛如一只展翅低头飞翔的鸟,其键线式结构表示如图,其中R 1、R 2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )| A. | 始祖鸟烯与乙烯互为同系物 | |
| B. | 若R 1=R 2=甲基,则其化学式为C 12H 16 | |
| C. | 若R 1=R 2=甲基,则始祖鸟烯的一氯代物有3种 | |
| D. | 始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则两反应的反应类型是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃 | |
| B. | 从苯的结构简式 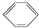 看,苯分子中含有碳碳双键,应属于烯烃 看,苯分子中含有碳碳双键,应属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 | |
| D. | 苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 四种常见元素的性质或结构信息如表.试根据信息回答有关问题.
四种常见元素的性质或结构信息如表.试根据信息回答有关问题.| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
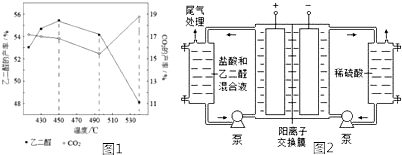
 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 78.5℃ | 100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L甲烷中含有的碳氢键数目为2NA | |
| B. | 常温下,1L0.1mol/L的Na2CO3溶液中含有OH-离子数为0.1NA | |
| C. | 常温常压下,28gN2、CO的混合气体中含有N2分子数为0.5NA | |
| D. | 标准状况下,22.4LCl2与足量NaOH溶液反应,转移的电子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com