
����Ŀ������һ�ݺ���FeCl3��FeCl2�������Ϊ�ⶨ���ɷֵĺ���������������ʵ�飺
ʵ��1���� ��ȡһ����������Ʒ������Ʒ�ܽ���
�� ���ܽ�����Һ�м���������AgNO3��Һ������������
�� ������������ϴ��������õ���ɫ����17.22 g��
ʵ��2���� ��ȡ��ʵ��1����ͬ��������Ʒ������Ʒ�ܽ���
�� ���ܽ�����Һ��ͨ��������Cl2��
�� ������������Һ�м���������NaOH��Һ���õ�����ɫ������
�� ������������ϴ�������������������������٣��õ���������4g��
�ش��������⣺
��1���ܽ���������õ��IJ���������___________________��
��2ʵ���ұ���FeCl2��Һʱͨ���������м��������Լ�_____________��_____________��
��3��ʵ��2ͨ������Cl2��Ŀ����_____________���漰�Ļ�ѧ��Ӧ�����ӷ���ʽ��____________________��
��4����ʵ��2�IJ������г�������ϴ�������ķ�����_____________��
��5������FeCl3��Һ��������Һ����ʱ��ͨ�����ܵõ�FeCl3���壬����ƽ������������ԭ��������ʽ��������������˵����______________________��
��6��FeCl3��Һ��������ֹѪ����Ҫ����ΪFeCl3��Һ��ʹѪҺ�۳������漰��������ԡ��������������˵������ȷ����_____________��
A����������������ֽ������������Ĥ
B���������Ӿ�������ı������������������ӻ������ӣ������糡�������������Ӿ����
C����Fe��OH��3�������Բ��������ЧӦ��CuSO4��Һ��ˮ�ȷ�ɢϵ���ܲ���������ЧӦ
D����Fe��OH��3�����еμ����ᣬ���ȳ��ֺ���ɫ���������������ʧ
E���ڵ�������Һ�м���ϡ��CuSO4��Һ����ʹ����������
��7��ͨ��ʵ���������ݣ����������Ʒ��FeCl3��FeCl2����������֮��Ϊ_________��
���𰸡���1���ձ���������
��2��ϡ���� ����
��3����Fe2+ȫ��ת��ΪFe3+ 2Fe2++Cl2=2Fe3++2Cl��
��4��ȡ�������һ�ε�ϴ��Һ���Թ��У����Թ�����Һ�μ����������ữ��AgNO3��Һ����δ���ְ�ɫ����˵����ϴ��
��5��FeCl3 ��ˮ�д�������ƽ�� FeCl3+3H2O![]() Fe��OH��3+3HCl���ڼ��������£�����HCl�ӷ���������Ũ�ȼ�С������ƽ�ⲻ�������ƶ���������ܵõ�FeCl3 ����
Fe��OH��3+3HCl���ڼ��������£�����HCl�ӷ���������Ũ�ȼ�С������ƽ�ⲻ�������ƶ���������ܵõ�FeCl3 ����
��6��E��7��2��3
��������
�����������1���ܽ����õ�������Ϊ�ձ�������������2��FeCl2�ױ������е�����������FeCl3������Һ�м����������ۣ�ʹFeCl3����ת��ΪFeCl2��Ϊ�˷�ֹFeCl2��Һˮ�⣬���������ᣬ������ˮ�⣬��ֹ����ʣ���3��Cl2��FeCl2��������FeCl3��Cl2+2FeCl2=2FeCl3��ʵ��Ϊ2Fe2+ + Cl2 = 2Fe3+ + 2Cl������4��������ʱ������Ҫ��ȷ����������ʲô���ʣ������Ȼ��ƺ���������Ӧ�����Ȼ��������������ƣ���˳���������������Na+��Cl-����������Ƿ�ϴ�Ӹɾ���ֻҪ����ϴ�Ӻ����Һ���Ƿ���Na+��Cl-�е�һ�־Ϳ�����������һ�ε�ϴ��Һ��Ȼ���Ȼ��ƣ�������������Һ�ͻ���ֳ�������֮��˵����Һ��û���Ȼ��ƣ���5����ΪFeCl3��ˮ�⣬��HCl�ӷ������ȴٽ���FeCl3ˮ�⼰HCl�Ļӷ������Բ��ܵõ�FeCl3��������6��A����������ֱ������1��100nm֮�䣬���������ֽ������������Ĥ��A��ȷ��B���������Ӿ�������ı������������������ӻ������ӣ�������糡������������������������������Ӿ����B��ȷ��C����Fe��OH��3�������Բ��������ЧӦ��CuSO4��Һ��ˮ�ȷ�ɢϵ���ܲ���������ЧӦ��C��ȷ��D���������м����������ᡢ��Σ����кͽ��������ĵ�ɣ�ʹ���巢���۳���������Fe��OH��3�����еμ����ᣬ���ȳ��ֺ��ɫFe��OH��3�����������������ỹ���Fe��OH��3����������Ӧ������������D��ȷ��E��CuSO4�����ؽ����Σ���ʹ�����ʱ��ԣ�����������E����ȷ����7������![]() ����ʵ��������AgCl��nΪ
����ʵ��������AgCl��nΪ![]() mol = 0.12mol��ʵ��������Fe2O3��nΪ
mol = 0.12mol��ʵ��������Fe2O3��nΪ![]() mol = 0.025mol����FeCl3��FeCl2�����ʵ����ֱ�Ϊx mol��y mol������Cl��Fe�غ�3x mol+2y mol=0.12 mol��x mol+y mol=0.025 mol��2�����x = 0.02��y = 0.03����������Ʒ��FeCl3��FeCl2����������֮��ΪΪ2��3��
mol = 0.025mol����FeCl3��FeCl2�����ʵ����ֱ�Ϊx mol��y mol������Cl��Fe�غ�3x mol+2y mol=0.12 mol��x mol+y mol=0.025 mol��2�����x = 0.02��y = 0.03����������Ʒ��FeCl3��FeCl2����������֮��ΪΪ2��3��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����������Ļ�ѧԪ�ص���֤����ȷ���ǣ� ����
A. �����������������Ȼ��Ļ�ѧԪ���У�̼Ԫ�غ������
B. �ˡ�������ֲ�������Ļ�ѧԪ�ص��������ܴ�
C. ���������Ļ�ѧԪ��������Ȼ�綼�����ҵ�
D. �������Ȼ��Ļ�ѧԪ���������嶼�����ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⼰�仯����������������ͿƼ��ȷ��涼������Ҫ��Ӧ�á��ش��������⣺
��1���ⲻ������ˮ���������ڵ⻯����Һ�����ɶ�����ӣ���Ӧ���£�
��I2��s��+I-��aq��![]() I3-��aq����H<0����I2��s��+2I-��aq��
I3-��aq����H<0����I2��s��+2I-��aq��![]() I42-��aq��
I42-��aq��
��Ӧ����ƽ�ⳣ���ı���ʽΪK=____________���¶�����ʱ����Ӧ����ƽ�ⳣ����____________����������������С��������������
��2����������һ���¶��£��ɷ������¿��淴Ӧ��W��s��+I2��g��![]() WI2��g����ȷ��ȡ0.508g���0.736g�����ٷ�����50.0mL���ܱ������У�������ʹ�䷴Ӧ����ͼ�ǻ�������е�WI2���������ʵ�����ʱ��仯��ϵ��ͼ��[n��WI2����t]��������������0��t2ʱ������ķ�Ӧ�¶�Ϊ450��������������t2ʱ�̿�ʼ���ķ�Ӧ�¶�Ϊ530��
WI2��g����ȷ��ȡ0.508g���0.736g�����ٷ�����50.0mL���ܱ������У�������ʹ�䷴Ӧ����ͼ�ǻ�������е�WI2���������ʵ�����ʱ��仯��ϵ��ͼ��[n��WI2����t]��������������0��t2ʱ������ķ�Ӧ�¶�Ϊ450��������������t2ʱ�̿�ʼ���ķ�Ӧ�¶�Ϊ530��

���÷�Ӧ��H_________0������>������<������
����Ӧ�ӿ�ʼ��t1��t1=3min��ʱ���ڵ�ƽ������v��I2��= ____________
����450��ʱ���÷�Ӧ��ƽ�ⳣ��K=____________��
���ܹ�˵��������Ӧ�Ѿ��ﵽƽ��״̬����____________ ����ѡ����ĸ��
A.I2��WI2��Ũ�����
B.��λʱ���ڣ����������ĵ����ʵ����뵥�ʵ����ɵ����ʵ������
C.�����ڻ��������ܶȲ��ٸı�
D.����������ѹǿ�������仯
��3��I2O5�ǰ�ɫ��ĩ״���壬������������ʹH2S��CO��HC1���������ںϳɰ���ҵ�г���I2O5����������CO�ĺ�����
��֪����2I2��s��+5O2��g����2I2O5��s����H��-75.56kJmol-1
��2CO��g��+O2��g����2CO2��g����H��-566.0kJmol-1��
д��CO��g����I2O5��s����Ӧ������̬I2���Ȼ�ѧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����β����������ȼ�ϵ��Ϊ����ԭ���ⶨCO��Ũ��,��װ����ͼ��ʾ,�õ���е����Ϊ������-������,����O2-�����ڹ������NAMCON�������ƶ�������˵������ȷ����( )

A.��������ͨ���ĵ���Խ��,CO�ĺ���Խ��
B.����ʱ�����ɵ缫aͨ���������NAMCON����缫b
C.����ʱ�缫b������,�����ɵ缫a����缫b
D.��������������1 mol O2-ͨ��ʱ,����ת��2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѡ��3�����ʽṹ�����ʡ�X��Y��M��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2�Ǻ���ɫ���壻X����Ԫ�ؿ��γ�XH3��M�����ڱ��е縺������Ԫ�أ�Z��̬ԭ�ӵ�M����K���������3����R2�����ӵ�3d�������9�����ӡ���ش��������⣺
��1����̬Yԭ�ӵļ۵����Ų�ͼ��___________��Z���������е�һ��������������Ԫ����___________��Ԫ�����ƣ���
��2��XY2���ӵ����幹����___________��R2+��ˮ������[R��H2O��4]2+�У��ṩ�µ��ӶԵ�ԭ����___________��Ԫ�ط��ţ���
��3����֪XH3����R2+�γ������ӣ���XM3������R2+�γ������ӣ���ԭ����______________________��
��4��Y��R���γɵĻ����ᄃ�徧������ͼ��ʾ���þ���Ļ�ѧʽ��___________��������������ͼ��ʾ����þ����ܶ���___________g��cm��3����ʽ��������������С�������һλ����

��5��ͼ1��ʾij�ֺ����л�������Ľṹ���������4����ԭ�ӷֱ�λ�����������4�����㣨��ͼ2���������ڴ��ڿ�ǻ����Ƕ��ij���ӻ���Ӳ��γ�4���������ʶ�����з��ӻ������У��ܱ����л�������ʶ�����___________�����ţ���

a��CF4b��CH4c��NH4+d��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���� 0.50 mol/L NaOH ��Һ�� 0.50 mol/L H2SO4 ��Һ�����к��ȵIJⶨ��
��.���� 0.50 mol/L NaOH ��Һ
(1��ʵ���д�ԼҪʹ�� 245 mL NaOH ��Һ,��������Ҫ���� NaOH ���� g��
(2���ӱ���ѡ����� NaOH ��������Ҫ������ (���������

��.�ⶨ�к��ȵ�ʵ��װ����ͼ��ʾ��

(3��д��ϡ�����ϡ NaOH ��Һ��Ӧ��ʾ�к��ȵ��Ȼ�ѧ����ʽ (�к���Ϊ 57.3 kJ/mol����

���¶Ȳ��ƽ��ֵΪ__________��
��ʹ������ NaOH ��Һ��Ͼ��ȵ���ȷ������ (����ĸ����
A�����¶ȼ�С�Ľ��� B���ҿ�ӲֽƬ�ò���������
C����������ձ� D���������¶ȼ��ϵĻ��β������������ؽ���
�۽�����Ϊ 0.50 mol/L NaOH ��Һ�� 0.50 mol/L ������ܶȶ��� 1g/cm3���кͺ�������Һ�ı����� c = 4.18 J/(g�����������к��� �� H= ________(�������С�����һλ����
������ʵ������ 57.3 kJ/mol ��ƫ��������ƫ���ԭ�������__________(����ĸ����
A��ʵ��װ�ñ��¡�����Ч����
B����ȡ NaOH ��Һ�����ʱ���Ӷ���
C���ֶ�ΰ� NaOH ��Һ����ʢ�������С�ձ���
D�����¶ȼƲⶨ NaOH ��Һ��ʼ�¶Ⱥ�ֱ�Ӳ��� H2SO4 ��Һ���¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2CO(g��+O2(g��=2CO2(g�� ��H=-568kJ��mol-1
��H2(g��+1/2O2(g��=H2O(g�� ��H=-248kJ��mol-1
��֪ CO �� H2 �Ļ���� 1 mol �������г��ȼ�շų������� 272 kJ����û�������� CO �����������ʵ����ı�ֵΪ
A��1��1 B��3��37 C��2��1 D��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬŨ��(c)���¶�(T)����������������ˮ����Ӧ(��֪ˮ�ⷴӦΪ���ȷ�Ӧ)��˲ʱ����(v)���±��������ж�����ȷ����( )
| 0.600 | 0.500 | 0.400 | 0.300 |
318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
328.2 | 9.00 | 7.50 | a | 4.50 |
b | 2.16 | 1.80 | 1.44 | 1.08 |
A��a=6.00 B����ͬ�¶�ʱ������Ũ�ȼ���һ�������ʱ����ͬ
C��b��318.2 D��ͬʱ�ı䷴Ӧ�¶Ⱥ����ǵ�Ũ�ȣ�v���ܲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�ɷ�FeS2�������������̷���FeSO4��7H2O���Ĺ�ҵ����ʾ��ͼ������
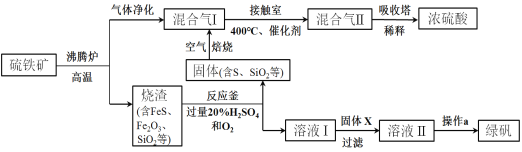
��1������¯�У���������з��鴦����Ŀ���� ��
��2���Ӵ����У���������Ҫ��Ӧ��SO2��O2�ķ�Ӧ���仯ѧ����ʽ�� ��
��3����Ӧ���У�����������Ӧת��Ϊ��ҺI���塣
�� �����е�FeS�ڷ�Ӧ���� ��������������������ԭ������
�� ��ҺI���������ʵĻ�ѧʽ�� ��
��4������a����Ҫ�����ǣ�����Ũ���� ������ϴ�ӡ�
��5��������������X����ѡ����������FeS2���� ��������XΪ��������FeS2��ʱ������ҺI�����X������Ӧ�����ӷ���ʽ����������
FeS2+![]() +
+![]() ===
===![]() Fe2++
Fe2++![]() SO42-+
SO42-+![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com