
有几个实验小组的同学,利用下图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质。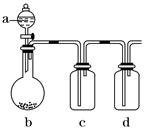
请你回答以下各组同学在交流实验设计方案中提出的问题:
Ⅰ.(1)若a:浓盐酸;b:高锰酸钾(其氧化性比二氧化锰强很多);c:红色鲜花瓣。在实验过程中c中的现象_____________________________________________________________。
d装置中盛放药品的作用是______________________________,请写出d中反应的离子方程式: ___________________________________________________________________。
(2)若a:稀盐酸;b:贝壳粉;c:饱和碳酸钠溶液;d:饱和Na2SiO3溶液。在实验过
程中,c中出现的现象是____________________。d中现象是____________,这说明
________________________________________________________________________。
Ⅱ.你认为四组同学在制取气体之前都应进行的操作是________________。你还可以利用此装置的a和b两部分制取的气体有(只写一种)_________________。
Ⅰ.(1) 花瓣褪色
吸收未反应的氯气,防止污染空气
Cl2+2OH-=Cl-+ClO-+H2O
(2)有白色沉淀析出 出现胶状物质 生成不溶性的硅酸,即硅酸的酸性弱于碳酸
Ⅱ.装置气密性检查 氧气(或二氧化硫)(合理答案均可)
解析试题分析:Ⅰ(1)氯气与水反应生成盐酸和次氯酸,干燥的氯气无漂白作用,氯气与水生成的次氯酸有漂白作用,由于氯气有毒,故用碱液吸收,红色鲜花瓣中有水能生成次氯酸,故答案为:花瓣褪色;吸收未反应的氯气,防止环境污染;Cl2+2OH-=Cl-+ClO-+H2O;(2)盐酸与贝壳粉(主要成分为碳酸钙)反应生成二氧化碳,二氧化碳与硅酸钠反应生成硅酸,由于硅酸是难溶于水的,故有白色沉淀析出;故答案为:有白色沉淀析出; 出现浑浊;苯酚的酸性弱于碳酸;Ⅱ制取气体之前都应进行的操作是装置气密性检查。装置的a和b组成的仪器属于固液不加热来制气类型,可以制备 氧气(或二氧化硫)。
考点:本题考查了气体的制备和气体性质的检验。


科目:高中化学 来源: 题型:单选题
下图装置可用于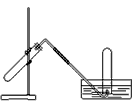
| A.用氯酸钾和少量二氧化锰,制取氧气 |
| B.用NH4Cl与Ca(OH)2,制取NH3 |
| C.用Cu和浓HNO3反应制取NO2 |
| D.用Cu和稀HNO3反应制NO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,应加热蒸馏,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是( )
| A.产品中有被蒸馏出的H2SO4 |
| B.有部分未反应的乙酸被蒸馏出来 |
| C.有部分未反应的乙醇被蒸馏出来 |
| D.有部分乙醇跟浓H2SO4作用生成乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。钙在加热时能与氮气、氢气反应。氢化钙遇水立即反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,下图是模拟制取装置。
(1)下列关于氢化钙的叙述正确的是 (选填序号)。
a.氢化钙中阴离子的半径小于Li+的半径
b.氢化钙的式量小于溴化氢,因此前者的熔点小于后者
c.氢化钙也能与盐酸反应生成氢气
d.氢气常用作还原剂,只具有还原性
(2)上图A装置中制备氢气所用的酸溶液最好选用 (选填序号)。
a.稀盐酸 b.稀硫酸 c.稀硝酸 d.均可以
(3)装置D中竖直导管的作用是 。
(4)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是 。加热C装置前要对H2验纯,验纯的操作是 。
(5)甲同学认为只要装置合理、操作规范就可以排除生成 (选填序号)。
a.Ca3N2 b.CaO c.Ca(OH)2
(6)乙同学用下图装置测定制得的氢化钙的纯度。他称取48g样品,与足量的水反应,恒温时,注射器量出产生的气体为48.16 L(已换算为标准状况)。假设钙只与氢气发生了反应,请根据乙同学的实验数据计算氢化钙的纯度(写出计算过程) 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯气和氮氧化物都是重要的化工原料,但进入大气后,都对环境造成污染。
【Ⅰ】已知:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+ 8 H2O,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是 。(选填A或B或C)
(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式: 。
(3)常用NaOH溶液吸收氯气防止污染。写出该反应的离子方程式 。
【Ⅱ】已知:NO2+NO+2NaOH=2NaNO2+H2O,可用氢氧化钠溶液可以吸收废气中的氮氧化物。
(1)在该反应中,氧化剂是 。
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气无污染的物质。写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铬及其化合物在现代工业上的应用广泛,可用于电镀,鞣制羊毛,皮革;铬还用于照相材料,胶版印刷及化工触媒剂等。但化工废料铬渣对人体健康有很大危害。
Ⅰ:某工厂对制革工业污泥中Cr(III)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | —— | —— | 4.7 | —— |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq) 的溶度积Ksp= c(Cr3+)? c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
的溶度积Ksp= c(Cr3+)? c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有A、B、C、D、E、F六种物质,它们之间相互转化关系如图所示(条件及部分产物未标出)。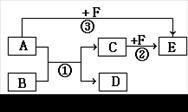
(1)若A、D为气体,都能使澄清的石灰水变浑浊;B、F做焰色反应,透过蓝色钴玻璃观察为紫色, B、C为正盐,F的溶液为紫红色。则C和F在酸性溶液中发生反应②的离子方程式为 。
(2)若1 mol A分子中含有3 mol极性共价键, B、C、F都是短周期元素组成的非金属单质;常温下,只有D为固体,其它为气体。则反应③的化学方程式为 。
某同学设计了如图所示装置(夹持仪器省略)进行上述(2)中物质B的化学性质探究。
①你认为此装置设计是否合理?若不合理如何改进: 。(若合理此问不答)
②Ⅱ中产生的现象是 。
③反应几分钟后,检验Ⅲ中可能含有的金属阳离子的实验操作是 。
④通过以上探究,气体B的主要化学性质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(11分)苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
已知:苯甲酸相对分子质量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热,溶解,Ⅰ | 得到白色晶体和无色溶液 | ———— |
| ② | 取少量滤液于试管中, Ⅱ | 生成白色沉淀 | 滤液含有Cl- |
| ③ | 干燥白色晶体, Ⅲ | Ⅳ | 白色晶体是苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
工业上以黄铜矿(主要成分是CuFeS2,杂质不溶于水和酸)为原料,制备蓝色晶体G,其化学式为[Cu(NH3)4]SO4·H2O,涉及流程如下:
已知25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表:
(1)黄铜矿在空气中焙烧能生成铁和铜的低价硫化物,写出其反应的化学方程式 ;
(2)试剂X的化学式为 ,双氧水的作用是 ;
(3)常温下,0.1 mol/L试剂Y的pH=11,则该温度下,试剂Y的电离常数为 ,用pH试纸测该溶液pH值的方法是 ;
(4)在溶液N中加入乙醇的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com