
【题目】下列物质可保持在带橡胶塞的无色细口玻璃瓶的是
A.金属钠B.氢氟酸C.浓硫酸D.碳酸钠溶液
科目:高中化学 来源: 题型:
【题目】下列实验不能达到目的的是
A. 用过量NaOH溶液除去镁粉中的铝粉 B. AlCl3溶液和氨水制备Al(OH)3沉淀
C. 用盐酸和AgNO3溶液鉴定Cl- D. 用加热的方法鉴别Na2CO3和NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,在体积不变的密闭容器中,有可逆反应X(s)+2Y(g) ![]() 2Z(g) △H<0,下列说法—定正确的是
2Z(g) △H<0,下列说法—定正确的是
A. 0.2molX和0.4molY充分反应,Z的物质的量可能会达到0.35mol
B. 从容器中移出部分反应物X,则正反应速率将下降
C. 当△H不变时,反应将达到平衡
D. 向反应体系中继续通入足量Y气体,X有可能被反应完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu

(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是___________
②Cu电极上发生的电极反应式为__________
③原电池工作时,盐桥中的_____离子(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是______极;
②图丙中的②线是_________离子的变化。
③当电子转移为2mol时,向乙烧杯中加入_____L5mol/LNaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________
Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应,若生成硫酸钡沉淀的质量比为1∶2∶3,则三种硫酸盐的物质的量浓度之比为( )
A. 1∶2∶3 B. 1∶6∶9 C. 1∶3∶3 D. 1∶3∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用原电池原理可以处理硫酸工业产生的SO2尾气。现将SO2 通入如图装置(电极均为惰性材料)进行实验。下列说法不正确的是
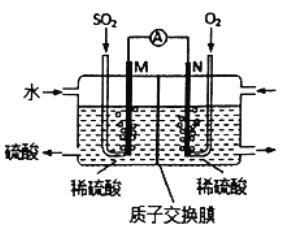
A. M极为负极,电极上发生氧化反应
B. 溶液中H+移向N区,SO42-移向M区
C. N极发生的电极反应为O2+4H++4e-=2H2O
D. 相同条件下,M、N两极上消耗的气体体积之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某实验小组为探究ClO-、I2、SO![]() 在酸性条件下的氧化性强弱,设计实验如下:
在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:__________________________。
(2)实验②的化学反应中转移电子的物质的量是___________________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO![]() 的氧化性由弱到强的顺序是________________。
的氧化性由弱到强的顺序是________________。
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由3种常见短周期元素组成的化合物A,相对分子质量为119,能与水剧烈反应,生成2种酸性气体的混合气体B。现对化合物A进行下列实验,假设各步反应均完全,反应中气体完全逸出。
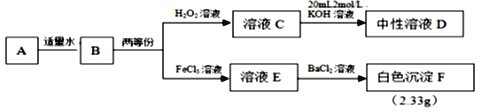
请回答:
(1)D中溶质的化学式_____________________,H2O2的电子式_______________。
(2)A和水反应的化学方程式___________________________________________。
(3)B→E的离子方程式______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com