
| A£® | ±½£Ø±½·Ó£© ¼ÓÅØäåĖ®£¬Õńµ“£¬·ÖŅŗ | |
| B£® | ø£¶ūĀķĮ֣ؼ×Ėį£© ¼Ó“æ¼īČÜŅŗ£¬·ÖŅŗ | |
| C£® | ŅŅ“¼£ØŅŅĖį£© ¼ÓNaOHČÜŅŗ£¬¹żĀĖ | |
| D£® | ŅŅĖįŅŅõ„£ØŅŅĖį£© ¼Ó±„ŗĶNa2CO3ČÜŅŗ£¬·ÖŅŗ |
·ÖĪö A£®äå”¢Čżäå±½·Ó¾łŅ×ČÜÓŚ±½£»
B£®¼×ĖįÓė“æ¼ī·“Ó¦ŗó£¬Óėø£¶ūĀķĮÖ²»·Ö²ć£»
C£®ŅŅĖįÓėNaOH·“Ó¦ŗó£¬ÓėŅŅ“¼»„ČÜ£»
D£®ŅŅĖįÓėĢ¼ĖįÄĘ·“Ó¦ŗó£¬ÓėŅŅĖįŅŅõ„·Ö²ć£®
½ā“š ½ā£ŗA£®äå”¢Čżäå±½·Ó¾łŅ×ČÜÓŚ±½£¬ŅżČėŠĀŌÓÖŹ£¬²»ÄܳżŌÓ£¬Ó¦Ń”NaOHČÜŅŗ”¢·ÖŅŗ³żŌÓ£¬¹ŹA“ķĪó£»
B£®¼×ĖįÓė“æ¼ī·“Ó¦ŗó£¬Óėø£¶ūĀķĮÖ²»·Ö²ć£¬²»ÄÜ·ÖŅŗ·ÖĄė£¬Ó¦Ń”ÕōĮó·Ø·ÖĄė£¬¹ŹB“ķĪó£»
C£®ŅŅĖįÓėNaOH·“Ó¦ŗó£¬ÓėŅŅ“¼»„ČÜ£¬²»ÄܹżĀĖ·ÖĄė£¬Ó¦Ń”ÕōĮó·Ø·ÖĄė£¬¹ŹC“ķĪó£»
D£®ŅŅĖįÓėĢ¼ĖįÄĘ·“Ó¦ŗó£¬ÓėŅŅĖįŅŅõ„·Ö²ć£¬Č»ŗó·ÖŅŗæɳżŌÓ£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ·ÖĄėĢį“棬ĪŖøßĘµæ¼µć£¬°ŃĪÕÓŠ»śĪļµÄŠŌÖŹ”¢·¢ÉśµÄ·“Ó¦¼°»ģŗĻĪļ·ÖĄėŌĄķµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Na+”¢Ba2+”¢Cl-”¢SO42- | B£® | Na+”¢Ba2+”¢AlO2-”¢NO3- | ||
| C£® | NH4+”¢K+”¢Cl-”¢NO3- | D£® | Na+”¢K+”¢NO3-”¢SiO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŌĢ¼°ōĪŖĮ½¼«µē½āĒāŃõ»ÆÄĘČÜŅŗ | B£® | ĻņĻ”ŃĪĖįÖŠµĪ¼ÓNaOHČÜŅŗ | ||
| C£® | ŅŌĢ¼°ōĪŖĮ½¼«µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗ | D£® | ĻņĒāŃõ»ÆÄĘČÜŅŗÖŠ¼ÓĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé·½°ø | ŹµŃéĻÖĻó |
| ¢ŁÓĆÉ°Ö½²ĮŗóµÄĆ¾“ųÓė·ŠĖ®·“Ó¦ŌŁĻņ·“Ó¦ŅŗÖŠµĪ¼Ó·ÓĢŖ | A£®ø”ÓŚĖ®Ćę£¬ČŪ³ÉŠ”Ēņ£¬ŌŚĖ®ĆęÉĻĪŽ¶ØĻņŅʶÆĖęÖ®ĻūŹ§£¬ČÜŅŗ±ä³ÉŗģÉ« |
| ¢ŚĻņŠĀÖʵÄH2S±„ŗĶČÜŅŗÖŠµĪ¼ÓŠĀÖʵÄĀČĖ® | B£®²śÉś“óĮæĘųĢ壬æÉŌŚæÕĘųÖŠČ¼ÉÕ£¬ČÜŅŗ±ä³ÉĒ³ŗģÉ« |
| ¢ŪÄĘÓėµĪÓŠ·ÓĢŖŹŌŅŗµÄĄäĖ®·“Ó¦ | C£®·“Ó¦²»Ź®·Ö¾ēĮŅ£¬²śÉśĘųĢåæÉŅŌŌŚæÕĘųÖŠČ¼ÉÕ |
| ¢ÜĆ¾“ųÓė2mol•L-1µÄŃĪĖį·“Ó¦ | D£®¾ēĮŅ·“Ó¦£¬²śÉśµÄĘųĢåæÉŅŌŌŚæÕĘųÖŠČ¼ÉÕ |
| ¢ŻĀĮĢõÓė2mol•L-1µÄŃĪĖį·“Ó¦ | E£®Éś³É°×É«½ŗד³Įµķ£¬¼Ģ¶ų³ĮµķĻūŹ§ |
| ¢ŽĻņĀČ»ÆĀĮČÜŅŗÖŠµĪ¼ÓĒāŃõ»ÆÄĘ | F£®Éś³Éµ»ĘÉ«³Įµķ |
| ŹµŃé·½°ø £ØĢīŠņŗÅ£© | ŹµŃéĻÖĻó £ØĢīŠņŗÅ£© | ÓŠ¹Ų»Æѧ·½³ĢŹ½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
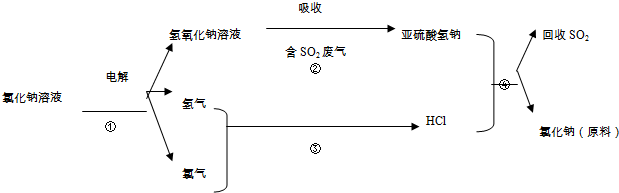
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| Ń” Ļī | ²Ł×÷ | ĻÖĻó | ½įĀŪ |
| A | ĻņĻ”µÄ±½·ÓĖ®ČÜŅŗÖŠµĪ¼ÓÅØäåĖ® | Éś³É°×É«³Įµķ | ²śĪļČżäå±½·Ó²»ČÜÓŚĖ® |
| B | µķ·ŪŗĶĻ”ĮņĖį»ģŗĻ¹²ČČŗó£¬ŌŁ¼ÓÉŁĮæŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ | ²śÉśŗģÉ«³Įµķ | µķ·ŪĖ®½āæÉÉś³ÉĘĻĢŃĢĒ |
| C | äåŅŅĶéŗĶĒāŃõ»ÆÄĘČÜŅŗ³ä·Ö·“Ó¦ŗó£¬ÓĆ×ćĮæĻ”ĻõĖįĖį»Æ£¬ŌŁ¼ÓČėĻõĖįŅųČÜŅŗ | Éś³Éµ»ĘÉ«³Įµķ | äåŅŅĶéÖŠŗ¬ÓŠäåŌŖĖŲ |
| D | ½«äåĖ®¼ÓČė±½ÖŠ²¢³ä·ÖÕńµ“ | äåĖ®ĶŹÉ« | ±½Óėäå·¢ÉśĮĖČ”“ś·“Ó¦ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
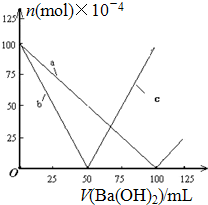
| A£® | ĒśĻßa±ķŹ¾Ba2+µÄĪļÖŹµÄĮæµÄ±ä»Æ | |
| B£® | ĒśĻßc±ķŹ¾OH-µÄĪļÖŹµÄĮæµÄ±ä»Æ | |
| C£® | ¼ÓČėBa£ØOH£©2ČÜŅŗ50mLŹ±·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O | |
| D£® | ¼ÓČėBa£ØOH£©2ČÜŅŗ“óÓŚ50mLŗ󣬷“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗOH-+H+ØTH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
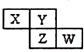 X”¢Y”¢Z¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚÖÜĘŚ±ķÖŠĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£®ČōYŌ×ÓµÄ×īĶā²ćµē×ÓŹĒÄŚ²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
X”¢Y”¢Z¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚÖÜĘŚ±ķÖŠĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£®ČōYŌ×ÓµÄ×īĶā²ćµē×ÓŹĒÄŚ²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ZµÄĄė×Ó°ė¾¶Š”ÓŚYµÄĄė×Ó°ė¾¶ | |
| B£® | WµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ±ČZµÄĒæ | |
| C£® | ZµÄ·Ē½šŹōŠŌ±ČYµÄĒæ | |
| D£® | XÓėYŠĪ³ÉµÄ»ÆŗĻĪļ¶¼Ņ×ČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 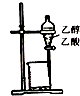 ³żČ„ŅŅ“¼ÖŠµÄŅŅĖį | B£® | 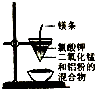 ÖĘȔɣĮ潚ŹōĆĢ | ||
| C£® | 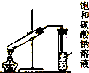 ÖĘČ”ŅŅĖįŅŅõ„ | D£® | 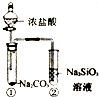 Ö¤Ć÷ĖįŠŌ£ŗŃĪĖį£¾Ģ¼Ėį£¾¹čĖį |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com