
请从图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。

(1)A极发生的电极反应式是_____________________·B极发生的电极反应式是_______________________;电解饱和食盐水的化学方程式是______________________。
(2)电源的M端应连接的电极为____________(A或B)极。
(3)设计上述气体实验装置时,各接口的正确连接顺序为:______________________________
__________________________________(填接口编号)。
(4)实验中,在盛有KI淀粉溶液的容器中发生反应的离子方程式为________________。
(5)已知饱和食盐水50mL,某时刻测得H2体积为56mL(标准状况)。此时溶液pH约为___________________。
(1)2 H++2e-=H2↑;(2分) 2 Cl--2e-= Cl2↑(2分)
2NaCl+2H2O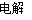 2NaOH+ H2↑+ Cl2↑(2分)
2NaOH+ H2↑+ Cl2↑(2分)
(2)B(2分)
(3)H、F、G、A、B、D、E、C(2分)
(4)Cl2+2I-=2 Cl-+2I2(2分)
(5)13(2分)
【解析】
试题分析:(1)A极应作阴极,H+放电,电极反应式是2 H++2e-=H2↑,B极是阳极,Cl-放电,电极反应式是2 Cl--2e-= Cl2↑电解饱和食盐水的化学方程式是2NaCl+2H2O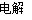 2NaOH+ H2↑+ Cl2↑;
2NaOH+ H2↑+ Cl2↑;
(2)M是正极应连接阳极B极,
(3)收集氢气用排水集气法,所以A→G→F→H,验证氯气的氧化性用淀粉碘化钾溶液,剩余氯气用氢氧化钠溶液吸收,所以B→D→E→C,整体连起来为H、F、G、A、B、D、E、C;
(4)在盛有KI淀粉溶液的容器中发生反应是氯气置换碘的反应,离子方程式为Cl2+2I-=2 Cl-+2I2
(5)n(H2)=0.0025mol,所以n(NaOH)=0.005mol,c(NaOH)=0.1mol/L,pH=13.
考点:考查电解饱和食盐水的实验所涉及的电解原理、装置连接、电极反应、pH的计算


科目:高中化学 来源:2015届山西省大同市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列叙述的说法不正确的是
A.金属的电化学腐蚀比化学腐蚀更普遍
B.用牺牲锌块的方法来保护船身
C.用铝质铆钉铆接铁板,铁板易被腐蚀
D.在镀件上电镀锌,用锌作阳极
查看答案和解析>>
科目:高中化学 来源:2015届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.拆开物质中的化学键一定需要吸收能量
C.应用盖斯定律,无法计算某些难以直接测量的反应焓变
D.化学反应都伴随着能量变化和其他各种现象的出现
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
取100 mL 2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A.加入适量的6mol/L的盐酸 B.用酒精灯适当加热
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
25℃时,把下列物质加入水中能促进水电离的是
A.NaCl B.HCI C.NH4Cl D.KOH
查看答案和解析>>
科目:高中化学 来源:2015届天津市和平区高二上学期期末考试化学试卷(解析版) 题型:选择题
今有两种盐的稀溶液,分别是a mol NaX溶液和b mol
NaX溶液和b mol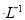 NaY溶液,下列说法不正确的是( )。
NaY溶液,下列说法不正确的是( )。
A.若a=b,pH(NaX)>pH (NaY),则相同浓度时,酸性HX>HY
B.若a=b,并测得c(X-)=c (Y-)+c(HY) ;则相同浓度时,酸性HX>HY
C.若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时, 酸性HX<HY
D.若两溶液等体积混合,测得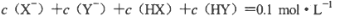
则可推出a+b=0.2 mol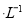
查看答案和解析>>
科目:高中化学 来源:2015届天津市和平区高二上学期期末考试化学试卷(解析版) 题型:选择题
下列事实可证明氨水是弱碱溶液的是( )。
A.氨水能被弱酸醋酸中和 B.铵盐受热易分解
C.氨水可以使酚酞试液变红 D.0.lmol/L氯化铵溶液的pH约为5
查看答案和解析>>
科目:高中化学 来源:2015届天津市南开区高二上学期期末考试化学试卷(解析版) 题型:选择题
实验①0.1 mol·L-1AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀C;②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;③向沉淀C中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
下列分析不正确的是
A.浊液a中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+C1-(aq)
Ag+(aq)+C1-(aq)
B.滤液b中不含Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高二教学评估(一)化学试卷(解析版) 题型:选择题
为检验某卤代烃(R—X)中的X元素,有下列实验操作:①加热煮沸;②加入AgNO3溶液;③取少量卤代烃;④加入稀HNO3酸化;⑤加入NaOH溶液;⑥冷却。正确操作的先后顺序为( )
A.③①⑤⑥④② B.③②①⑥④⑤
C.③⑤①⑥④② D.③⑤①⑥②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com