
科目:高中化学 来源:2015-2016学年河南省周口市高二下学期期中考试化学试卷(解析版) 题型:填空题
写出下列反应的方程式
(1)乙醇的催化氧化反应方程式
(2)乙醛与银氨溶液反应的方程式
(3)实验室制取乙烯的反应方程式
(4)乙酸乙酯在酸性条件下的水解反应方程式
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二下第十二周练化学卷(解析版) 题型:选择题
下列叙述中正确的是
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.非极性分子中,一定含有非极性共价键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
已知七种短周期元素a~g的有关信息如下表所示:
元素编号 | a | b | c | d | e | f | g |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -2 | +3 | -2 | +3 | +1 | +1 |
下列推断不正确的是
A.氢化物稳定性的强弱:b>d B.金属性的强弱:f<g
C.元素e的氧化物只能与酸反应 D.最高价氧化物对应的水化物的碱性:e<g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
下列各种规律描述正确的是
A.第ⅠA 族元素单质的熔点随着原子序数递增而升高
B.卤族元素单质的熔点随着原子序数递增而升高
C.第ⅤA族元素的气态氢化物沸点随着原子序数递增而升高
D.第三周期元素形成的简单离子半径随着原子序数递增而增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:填空题
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为__________________________;
(2)A中的碳原子是否都处于同一平面?____________(填“是”或“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。

(a)反应②的化学方程式为__________________________________________;
(b)C的化学名称是__________________________________________ ;
(c)E2的结构简式是__________________________________________ ;
(d)④、⑥的反应类型依次是______________________ , ____________________ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:选择题
有机物A、B只可能烃或烃的含氧衍生物,等物质的量的A、B完全燃烧时,消耗氧气的量相等,则A、B的相对分子质量相差不可能为(n为正整数)
A.8n B.14n C.18n D.44n
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:填空题
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+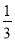 CO(g)═
CO(g)═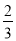 Fe3O4(s)+
Fe3O4(s)+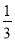 CO2(g)△H2
CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为__________(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为__________,该温度下若测得固体混合物中m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为__________(设其它固体杂质中不含Fe、O元素).
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0.在T℃,106Pa时将lmolCO和3molH2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g)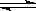 CH4(g)+H2O(g)达到平衡的是__________(填序号).
CH4(g)+H2O(g)达到平衡的是__________(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为__________;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为__________;
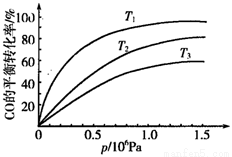
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是__________,理由是__________。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下表是3种物质在水中的溶解度(20℃),下列说法正确的是
物质 | MgCl2 | Mg(OH)2 | MgCO3 |
溶解度(g/100 g) | 54.6 | 0.000 84 | 0.039 |
A.已知MgCO3的Ksp=2.14×10-5,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=2.14×10-5
B.除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液
C.将式量的表中三种物质与足量水混合,充分加热、灼烧,最终的固体产物相同
D.用石灰水处理含有Mg2+和HCO3-,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com