
【题目】元素X形成的离子与镁离子的核外电子排布相同,且X的离子半径小于负二价氧离子的半径.X元素可能为( )
A.Ne
B.N
C.Na
D.K
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某科研小组研究镉、铜对河蚌过氧化氢酶活性的影响,用一定浓度的镉、铜处理河蚌一段时间后,测得河蚌过氧化氢酶活性如表所示.
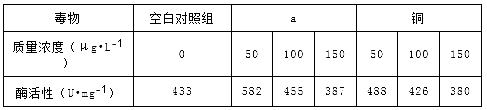
请回答下列问题:
(1)表中a应是 。
(2)请列举本实验需要控制的无关变量: 。(至少写出两个)
(3)进行过氧化氢酶活性测定时,选过氧化氢为底物,用一定条件下单位时间的 来表示。
(4)若测定镉和铜对河蚌过氧化氢酶活性的综合影响作用,本实验应如何完善? 。
(5)能否用河蚌过氧化氢酶作为实验材料来探究温度对酶活性的影响?为什么? 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种有机物以一定比例混合,一定条件下在a L O2(足量)中充分燃烧恢复到原状态,再通过过量的过氧化钠,得到气体仍是a L,下列组合中符合此条件的是( )
A.CH4、C2H4
B.CH3CH2OH,CH3COOH
C.C2H6、HCHO
D.HCOOH,CH3COOCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列有关说法正确的是( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1mol氦气含有的原子数为2NA
C.71gCl2所含原子数为2NA
D.23g钠在化学反应中失去电子数目为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 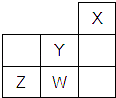
A.Y的原子半径在同周期主族元素中最大
B.W的非金属性比Z的弱
C.Z的气态氢化物的稳定性在同主族元素中最强
D.W的最高价氧化物对应的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国世界卫生组织经过严密的科学分析,认为我国的铁锅是最理想的炊具,并向全世界大力推广,其主要原因是( )
A. 铁锅价格便宜B. 铸铁锅的铁熔点高
C. 使用铁锅烹饪的食物中留有铁元素D. 铁锅含有有机物必含的碳元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( ) 实验后的记录:
①Zn为正极,Cu为负极
②Cu极上有气泡产生,发生还原反应
③SO42﹣向Zn极移动
④若有0.5mol电子流经导线,则产生5.6L气体
⑤电流的流向是:Cu→Zn
⑥负极反应式:Cu﹣2e﹣═Cu2+ , 发生氧化反应.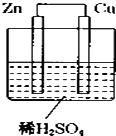
A.②④⑤
B.②③⑤
C.①④⑥
D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在指定的环境中一定能大量共存的是( )
A.常温下,在c(H+)/c(OH﹣)=1×1012的溶液中:I﹣、Cl﹣、NO ![]() 、Na+
、Na+
B.在能使石蕊变红色的溶液中:Na+、S2﹣、SO ![]() 、CO
、CO ![]()
C.在加入铝粉能产生H2的溶液中:NH ![]() 、Na+、NO
、Na+、NO ![]() 、Cl﹣
、Cl﹣
D.常温下由水电离出的c(H+)=1×10﹣12 mol?L﹣1的溶液中:K+、Cl﹣、NO ![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阴离子Xn﹣1含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是( )
A.![]() (N﹣a) mol
(N﹣a) mol
B.![]() (n+A)mol
(n+A)mol
C.![]() (N+n) mol
(N+n) mol
D.![]() (A﹣N+n) mol
(A﹣N+n) mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com